Parkinson’s disease (PD) is a relentless, progressive neurodegenerative disease characterized by the aggregation of misfolded α-synuclein proteins, which form Lewy bodies within dopaminergic neurons in the substantia nigra. This buildup ultimately leads to neuronal destruction.1,2
Beyond the visible symptoms, PD has also been found to disrupt multiple intracellular pathways, particularly those related to autophagy and mitophagy, contributing to a gradual decline in motor functions over many years. With more than 10 million people affected worldwide and United States healthcare costs exceeding $52 billion annually, the need for earlier and more precise diagnostics is more crucial than ever.3,4
|
Explore the Parkinson's antibody sampler kit, which contains reagents to many of the markers mentioned in this blog: |
|
There are currently no definitive diagnostics available for Parkinson’s. Instead, neurologists are reliant on patient history, motor symptoms, imaging, and response to therapeutics. But what if we could detect the disease before major symptoms appear? This is where biomarkers—both protein and genetic—come into play. They can help identify reliable biological signals early in disease progression and reveal the cellular and molecular mechanisms of PD etiology.
<Jump to the product list at the end of this blog>
Lewy Body-Related Proteins
Lewy bodies are an aggregate of misfolded proteins that disrupt several neuronal processes, including synaptic release and mitochondrial function. At the heart of this dysfunction is α-synuclein, the primary protein linked to PD.
#1: α-Synuclein
α-synuclein is a presynaptic protein involved in vesicle trafficking. When misfolded, however, it forms Lewy bodies―one of the defining pathological features of Parkinson's. This protein has become an important biomarker for identifying PD, and for evaluating potential treatments.
In 2023, The Michael J Fox Foundation disclosed the α-synuclein seed amplification assay, which analyzes spinal fluid samples to detect misfolded α-synuclein. Impressively, the assay correctly identified 87% of PD patients prior to motor symptomology, sparking huge interest in monoclonal antibody therapies targeting α-synuclein, with several companies now investigating these treatments.5
#2: Phospho-α-Synuclein
Synuclein is one of the most researched proteins in Parkinson’s disease, and for good reason. More than 90% of the α-synuclein found in Lewy bodies is phosphorylated, making phosphorylated α-synuclein a strong indicator of PD. As this protein can be detected in cerebrospinal fluid, researchers are actively studying it as a potential biomarker and possible diagnostic for PD.6
|
Browse antibody products for assessing the phosphorylation status of α-synuclein: • PhosphoPlus® α-Synuclein (Ser129) Antibody Duet #29087 |
|
#3: DOPA Decarboxylase (DDC)
DOPA decarboxylase (DDC) is an enzyme that, as a homodimer, catalyzes the decarboxylation of L-DOPA to produce dopamine. Recently, DDC was found to be elevated in cerebrospinal fluid and urine of PD patients, and elevated DDC levels could differentiate between PD and Alzheimer's disease patients.7 As such, DDC is a potential biomarker that could be measured to differentiate between PD and other neurodegenerative disorders.
#4: Glucocerebrosidase (GCase/GBA)
Originally linked to Goucher’s Disease, GCase has attracted interest in PD research due to its close association with Lewy body formation. Mutations in the GBA gene, which encodes GCase, are considered significant risk factors for both PD and Lewy body dementia.
Western blot (WB) analysis of extracts from immortalized gba+/+ and gba-/- mouse neurons using GCase/GBA (E2R1L) Rabbit mAb #88162 (upper) or β-Actin (D6A8) Rabbit mAb #8457 (lower). Immortalized gba+/+ and gba-/- mouse neurons kindly provided by Dr. Ellen Sidransky, MD at the National Human Genome Research Institute of the National Institutes of Health.
GCase is a lysosomal enzyme responsible for breaking down glycolipids. When mutations occur in GBA, this process is disrupted, contributing to α-synuclein aggregation—a hallmark of PD. Given its critical role, GBA gene replacement therapy is being explored as a potential treatment, with one clinical trial (NCT04127578) currently underway.8
Mitochondrial Regulation
Mitochondria are highly efficient producers of ATP. They are constantly recycled through fission, fusion, and mitophagy, processes that ensure a supply of healthy mitochondria. However, in PD, Lewy bodies disrupt these processes, leading to mitochondrial dysfunction—a major contributor to neuronal damage. Several proteins involved in mitochondrial regulation are influenced by Lewy bodies, making them valuable biomarkers and potential drug targets in PD research.
|
|
Explore related Antibody Sampler Kits: •Mitophagy Antibody Sampler Kit #43110 |
|
#5: Parkin
Parkin is a ubiquitin ligase that assists with mitochondrial recycling. When phosphorylated by PINK1, it helps remove damaged mitochondria through mitophagy. Mutations in the Parkin gene are linked to early-onset PD, highlighting its importance in disease progression. As such, the identification of Parkin is helpful for understanding the role of mitochondria in PD.9
#6: Phosphorylated PINK1 (Ser228)
PINK1 is a serine/threonine kinase that regulates healthy mitochondria. When mitochondria suffer damage, including oxidative stress, PINK1 is phosphorylated, in turn phosphorylating Parkin and initiating mitophagy. Mutations of PINK1 disrupt this process, leading to mitochondrial buildup and further neuronal damage. Because phosphorylated PINK1 serves as a marker for oxidative stress in neurons, it is an important tool for understanding PD pathology.9
#7 DJ-1
DJ-1 is a redox-sensitive protein that acts as an antioxidant, protecting mitochondria from oxidative stress. Early-onset PD has been associated with mutations in DJ-1.
 WB analysis of extracts from MEF wild-type, MEF DJ-1 (-/-), HeLa, and C6 cells using DJ-1 (D29E5) XP® Rabbit mAb #5933 (upper) and β-Actin (D6A8) Rabbit mAb #8457 (lower). (MEF wild-type and MEF DJ-1 (-/-) cells were kindly provided by Dr. Philipp Kahle, University of Tübingen, Germany).
WB analysis of extracts from MEF wild-type, MEF DJ-1 (-/-), HeLa, and C6 cells using DJ-1 (D29E5) XP® Rabbit mAb #5933 (upper) and β-Actin (D6A8) Rabbit mAb #8457 (lower). (MEF wild-type and MEF DJ-1 (-/-) cells were kindly provided by Dr. Philipp Kahle, University of Tübingen, Germany).
Neuronal Health & Maintenance
Several proteins are involved in removing misfolded proteins and maintaining neuronal homeostasis. When these processes break down, neurodegenerative diseases like PD can develop. Several key proteins play a role in protecting neurons and ensuring proper waste removal, while astrocytes, the brain’s support cells, also influence neuronal health and disease progression.
#8: UCHL1
Ubiquitin carboxyl-terminal hydrolase L1 (UCHL1) is a deubiquitinase enzyme involved in maintaining a pool of ubiquitin as substrates for degradation of other proteins. It is highly expressed in neurons, protecting them from misfolded proteins. However, its function is abrogated by mutation and oxidative stress. This protein has recently been implicated in PD pathophysiology.11

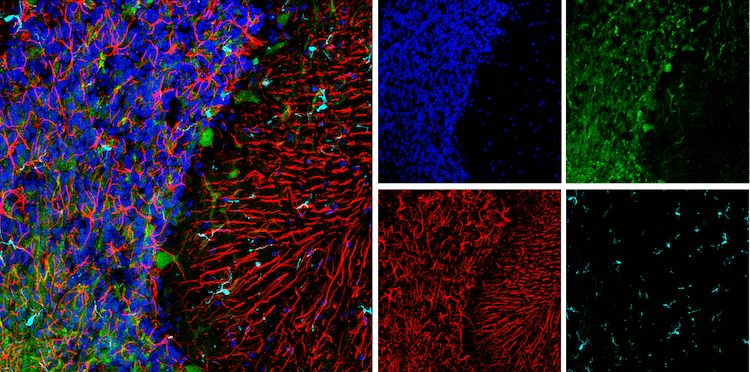
IF analysis of rat cerebellum using UCHL1 (D3T2E) XP® Rabbit mAb #13179 (green) and GFAP (E8S7G) Mouse mAb #95717 (red). After blocking free secondary antibody binding sites with Rabbit (DA1E) mAb IgG XP® Isotype Control #3900, the tissue was then labeled using Iba1/AIF-1 (E4O4W) XP® Rabbit mAb (Alexa Fluor® 647 Conjugate) #78060 (cyan pseudocolor) and ProLong® Gold Antifade Reagent with DAPI #8961 (blue).
#9: LRRK2
Leucine-rich repeat Kinase 2 (LRRK2) is essential for maintaining lysosomal function, which is crucial for cellular waste processing. Mutations in LRRK2 are one of the most common genetic causes of familial PD. These mutations increase kinase activity, leading to lysosomal dysfunction and neurite loss—both key contributors to PD progression. LRRK2 phosphorylates several GTPases of the Rab family, suggesting that LRRK2 might regulate intracellular membrane trafficking. Given its role in neuronal health, LRKK2 is a prime target for therapeutic development.12
 LRRK2 is highly expressed in 293T cells that were transfected with a construct expressing human LRRK2. The relationship between lysate protein concentration from mock-transfected cells and cells transfected with an expression construct encoding human LRRK2 and the absorbance at 450 nm using the PathScan® RP Total LRRK2 Sandwich ELISA Kit #69930 is shown in the figure. 293T cells were either transfected with a construct expressing wild-type human LRRK2 or mock-transfected, and then lysed.
LRRK2 is highly expressed in 293T cells that were transfected with a construct expressing human LRRK2. The relationship between lysate protein concentration from mock-transfected cells and cells transfected with an expression construct encoding human LRRK2 and the absorbance at 450 nm using the PathScan® RP Total LRRK2 Sandwich ELISA Kit #69930 is shown in the figure. 293T cells were either transfected with a construct expressing wild-type human LRRK2 or mock-transfected, and then lysed.
#10: VPS35
Vacuolar Protein Sorting 35 (VPS35), abundantly expressed in the brain, is a key component of the retromer complex―which is responsible for sorting and recycling transmembrane proteins. It assists with α-synuclein trafficking, and recycling, and maintenance of mitochondria. A specific p.D620N mutation in the VPS35 gene has been linked to late-onset familial PD. Thus, studying its expression and function can help identify new therapeutic targets for advanced PD.13
A Targeted Approach for PD Research
This toolbox represents a comprehensive, focused set of Parkinson's-related proteins that can aid scientists in the study of PD pathophysiology and offer potential biomarkers for diagnosis and eventual disease treatment.
| 標的 | 製品 | アプリケーション | 交差性 |
| α-Synuclein | α-Synuclein (E4U2F) XP® Rabbit mAb #51510 | WB, IP, IHC, IF | H, M, R |
| Phospho-α-Synuclein | Phospho-α-Synuclein (Ser129) (D1R1R) Rabbit mAb #23706 | WB, IP, IF | H, M, R |
| DDC | DDC (D6N8N) Rabbit mAb #13561 | WB, IP | H, M, R |
| DJ-1 | DJ-1 (D29E5) XP® Rabbit mAb #5933 | WB, IP, IF | H, M, R, Hm, Mk |
| GCase/GBA | GCase/GBA (E2R1L) Rabbit mAb #88162 | WB | H, M, R |
| LRRK2 | LRRK2 (D18E12) Rabbit mAb #13046 |
WB, IP | H, M, R |
| Parkin | Parkin (D4Z1W) Rabbit mAb #32833 | WB | H, M, R |
| PINK1 | PINK1 (D8G3) Rabbit mAb #6946 | WB, IP | H |
| UCHL1 | UCHL1 (D3T2E) XP® Rabbit mAb #13179 | WB, IHC, IF, F | H, M, R, Mk |
| VPS35 | VPS35 (E6S4I) Rabbit mAb #81453 | WB | H, M, R, Mk |
| ELISA Kits & Matched Antibody Pairs | |||
| α-Synuclein | Total α-Synuclein Matched Antibody Pair #39702 | ELISA | M, R |
| α-Synuclein | Pathscan® Total α-Synuclein Sandwich ELISA Kit #54269 | ELISA | M, R |
| LRRK2 | PathScan® RP Total LRRK2 Sandwich ELISA Kit #69930 | ELISA | H, M |
参考文献
- Dawson TM, Ko HS, Dawson VL. Genetic animal models of Parkinson's disease. Neuron. 2010;66(5):646-661. doi:10.1016/j.neuron.2010.04.034
- Sharma B, Shekhar H, Sahu A, et al. Epigenetic insights into prostate cancer: exploring histone modifications and their therapeutic implications. Front Oncol. 2025;15:1570193. Published 2025 Apr 28. doi:10.3389/fonc.2025.1570193
- Parkinson'sFoundation. Who Has Parkinson's? 2025 [cited 2025; Available from: https://www.parkinson.org/understanding-parkinsons/statistics.
- Willis AW, Roberts E, Beck JC, et al. Incidence of Parkinson disease in North America. NPJ Parkinsons Dis. 2022;8(1):170. Published 2022 Dec 15. doi:10.1038/s41531-022-00410-y
- Alfaidi M, Barker RA, Kuan WL. An update on immune-based alpha-synuclein trials in Parkinson's disease. J Neurol. 2024;272(1):21. Published 2024 Dec 12. doi:10.1007/s00415-024-12770-x
- Wang Y, Shi M, Chung KA, et al. Phosphorylated α-synuclein in Parkinson's disease. Sci Transl Med. 2012;4(121):121ra20. doi:10.1126/scitranslmed.3002566
- Shebl, N., Salama, M. Exploring dopa decarboxylase as an ideal biomarker in Parkinson’s disease with focus on regulatory mechanisms, cofactor influences, and metabolic implications. npj Biomed. Innov. 2025;2(2). https://doi.org/10.1038/s44385-024-00005-7
- Blandini F, Cilia R, Cerri S, et al. Glucocerebrosidase mutations and synucleinopathies: Toward a model of precision medicine. Mov Disord. 2019;34(1):9-21. doi:10.1002/mds.27583
- Kondapalli C, Kazlauskaite A, Zhang N, et al. PINK1 is activated by mitochondrial membrane potential depolarization and stimulates Parkin E3 ligase activity by phosphorylating Serine 65. Open Biol. 2012;2(5):120080. doi:10.1098/rsob.120080
- Repici M, Giorgini F. DJ-1 in Parkinson's Disease: Clinical Insights and Therapeutic Perspectives. J Clin Med. 2019;8(9):1377. Published 2019 Sep 3. doi:10.3390/jcm8091377
- Buneeva O, Medvedev A. Ubiquitin Carboxyl-Terminal Hydrolase L1 and Its Role in Parkinson's Disease. Int J Mol Sci. 2024;25(2):1303. Published 2024 Jan 21. doi:10.3390/ijms25021303
- Sosero YL, Gan-Or Z. LRRK2 and Parkinson's disease: from genetics to targeted therapy. Ann Clin Transl Neurol. 2023;10(6):850-864. doi:10.1002/acn3.51776
- Wu A, Lee D, Xiong WC. VPS35 or retromer as a potential target for neurodegenerative disorders: barriers to progress. Expert Opin Ther Targets. 2024;28(8):701-712. doi:10.1080/14728222.2024.2392700