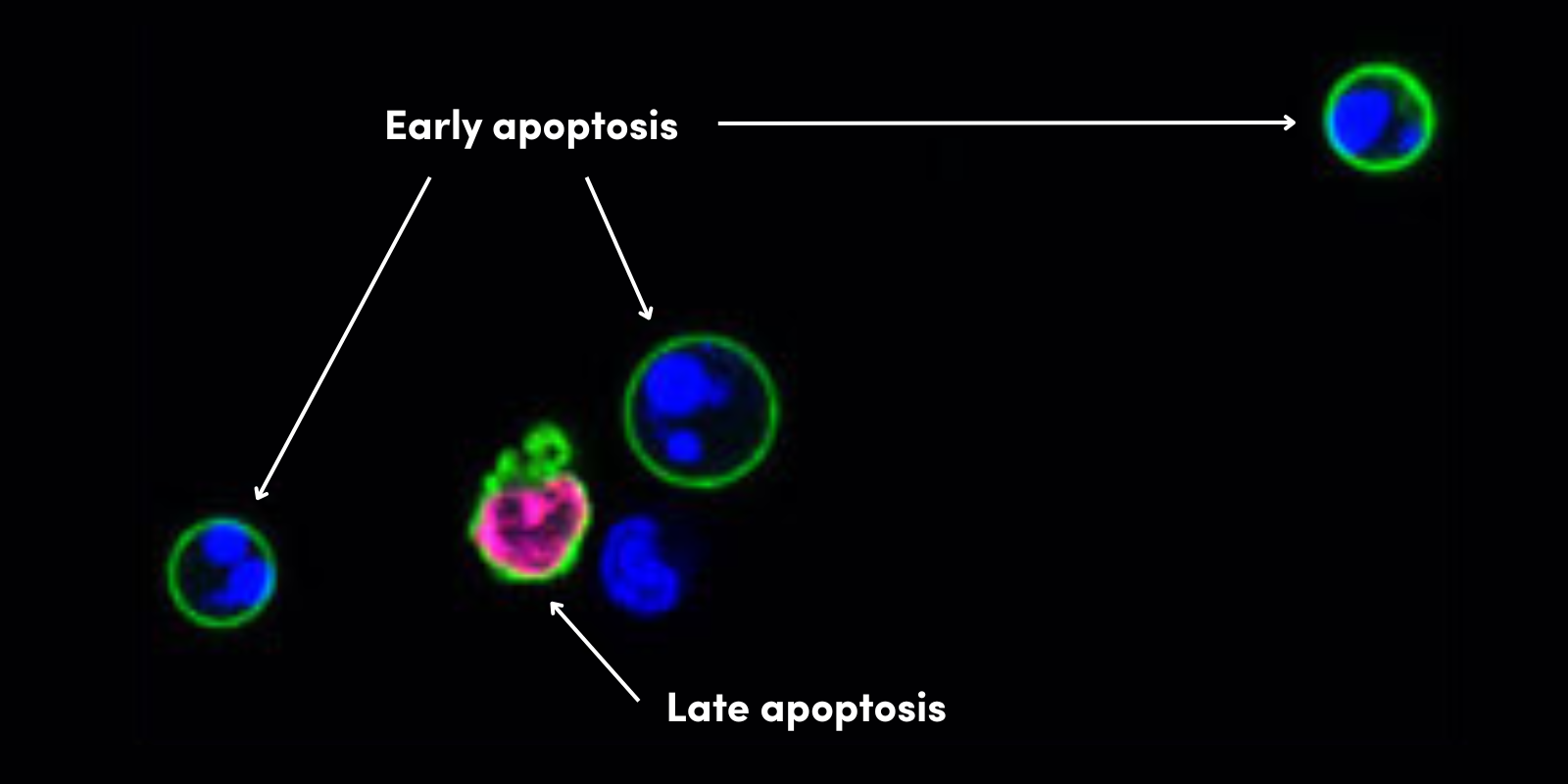
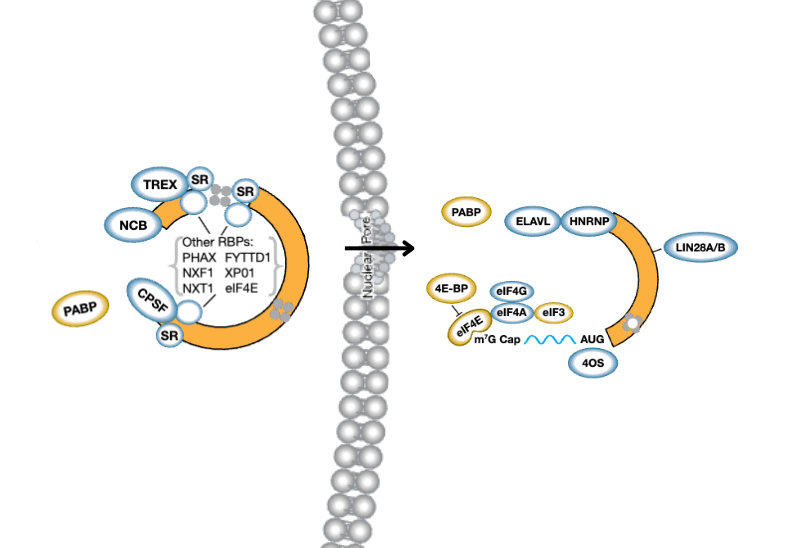
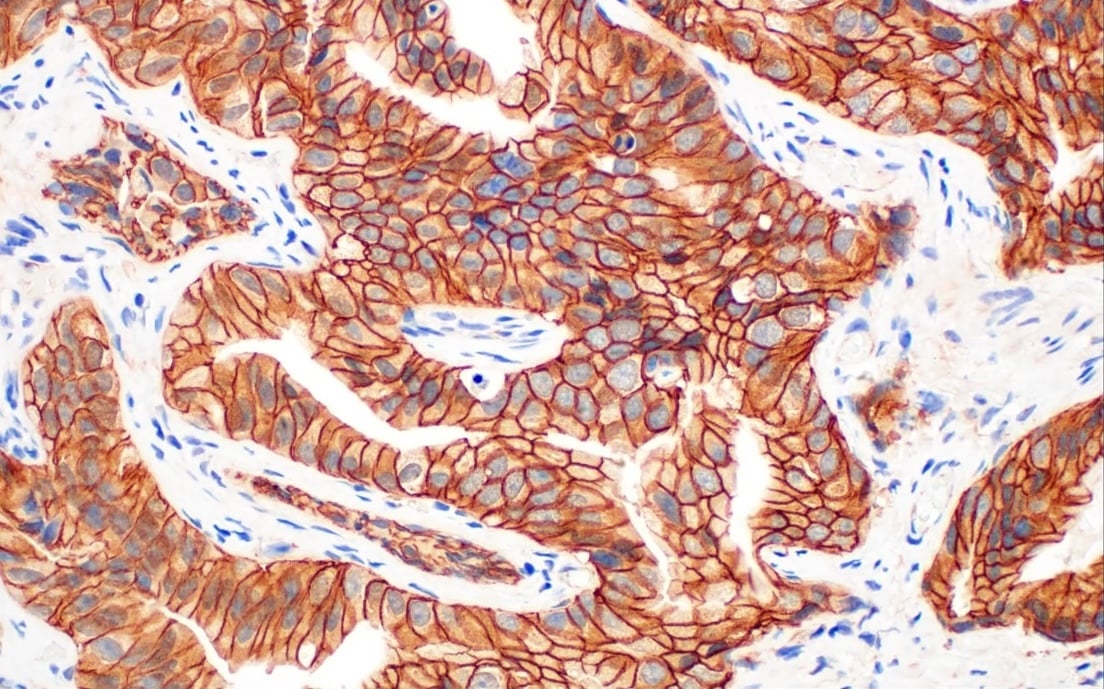
上皮間葉転換 (EMT) は、上皮細胞が元いた組織から離れた場所へ移動するための遊走能を獲得する生物学的プロセスです1。EMTは通常、創傷の治癒や組織の再構築といった重要な役割を担っています。しかし、がん化した細胞はこのメカニズムを乗っ取り、悪性度を増して、腫瘍の拡散を促進します。
EMTは、腫瘍の発達の初期段階および後期段階の両方に関与しています。腫瘍が転移し始めると、がん細胞はこのプロセスのサポートを受けて新たな環境に適応し、生存の可能性を向上させて、全身に悪性度の高い腫瘍を形成します。EMTは、腫瘍が臨床的に検出可能となる前に生じる可能性があり、早期診断や予防が非常に困難であるところが重要な点です。
このような複雑さに加え、EMTが生じたがん細胞は、化学療法や放射線治療、標的療法などに抵抗性を示すようになることが多く、初回治療後に再発する可能性が高くなります。
 |
本ブログで紹介するマーカーの多くに対する試薬が含まれる、関連するCST Antibody Samplerキットをご覧ください: • Epithelial-Mesenchymal Transition (EMT) Antibody Sampler Kit #9782 |
|
これらの問題をより深く理解して対処するために、研究者は様々なEMTマーカーの研究に注力しています。これらのマーカーは、がんの早期発見や転移の抑制、治療応答の向上の改善に大きく貢献する可能性があります。本ブログ記事では、最も注目を集めるEMTマーカーのいくつかを紹介し、これらが、がんの進行や治療抵抗性についての何を明らかにするのに役立つかを解説します。
<Jump to the product list at the end of this post>
EMTマーカーはがん研究にどのように用いられるのか
研究が進むにつれ、EMTは「全か無か」といった単純なプロセスではないことが明らかになってきています。むしろ、がん細胞は、上皮細胞と間葉系細胞の両方の性質を同時に持つ、様々な中間的な状態をとることが多々あります。この「細胞の可塑性」が、腫瘍細胞の多様な環境への適応、免疫系の回避、そしてがん治療などの様々なストレスへの抵抗を可能にします。EMTのこのような動的な性質から、EMTマーカーの特定と追跡はがん研究における強力なツールとなり、腫瘍がどのように進行および転移し、治療に対する抵抗性を持つようになるかに関する知見の取得につながります。
1. 細胞接着タンパク質への変化
EMTの明確な特徴の1つに、2種類の膜貫通型タンパク質E-cadherinとN-cadherinの発現量の変化があります。
|
|
|
EMTの間、強固な細胞接着の維持に寄与するE-Cadherinの発現量は減少する一方、N-Cadherinの発現量は増加します。この「カドヘリンスイッチ」により、がん細胞は原発腫瘍から剥離し、体内の別の部位へと遊走できるようになります2。両タンパク質は、EMTの主要なマーカーと考えられています。
その他の接着関連するタンパク質もまた、影響を受けます。ZO-1は、ジャンクション部位の膜貫通型タンパク質をアクチン細胞骨格に連結する表在性膜タンパク質 (アダプター) であり、EMT中に発現量が減少し、細胞の遊走の増加と転移能に寄与します。
同様に、タイトジャンクションの完全性に不可欠な膜貫通型タンパク質Occludinの発現量の減少も、細胞接着の弱まりとEMTの進行のシグナルになります。
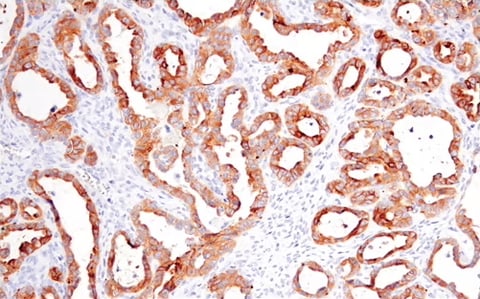
パラフィン包埋ヒト卵巣明細胞がん組織を、リコンビナントモノクローナル抗体Occludin (E6B4R) Rabbit mAb #91131を用いてIHCで解析しました。
別の膜貫通型タンパク質であるEpCAMも、多くのがん細胞で高発現しています。一般的なEMTマーカーではないものの、このタンパク質の発現量の増加もまた腫瘍組織の特定に役立ちます。
2. 細胞骨格タンパク質の異常
細胞骨格の変化もまた、EMTの指標となります。例えば、筋繊維芽細胞は通常、総称の修復をサポートする細胞骨格タンパク質であるAlpha-smooth muscle actin (SMA) を発現しています3。 しかし、がん細胞およびがん関連線維芽細胞 (CAF) もまた、EMT中にSMAを大量に産生しており、この量が多いほど予後不良となることが多々あります。

パラフィン包埋ヒト乳管がん組織を、リコンビナントモノクローナル抗体α-Smooth Muscle Actin (D4K9N) XP® Rabbit mAb #19245を用いてIHCで解析しました。
中間径フィラメントタンパク質であるVimentinも、重要なマーカーの1つです。その上流制御は、間葉状態を示唆し、移動性と浸潤性の上昇をサポートします。
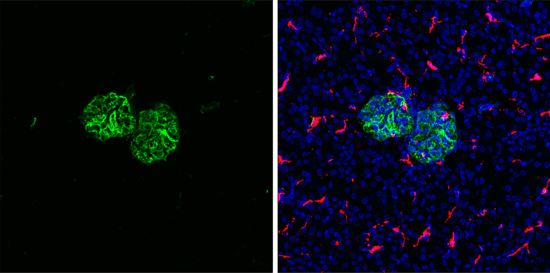
凍結固定マウス腎臓組織を、リコンビナントモノクローナル抗体Vimentin (D21H3) XP® Rabbit mAb #5741 (左、緑) とF4/80 (BM8.1) Rat mAb (右、赤)、ProLong® Gold Antifade Reagent with DAPI #8961 (右、青) を用いてIFで解析しました。
細胞外マトリックス (ECM) の主要なタンパク質であるFibronectinも、EMT中に著しく増加します。間葉系状態の指標となるFibronectinは、EMTのマーカーとして機能するだけでなく、細胞の接着や遊走、がん微小環境 (TME) との相互作用を促進することにより、腫瘍の発生や浸潤、転移に大きく寄与します。
3. EMTを制御する転写因子
上皮の特徴を抑制し、EMTの進行を可能にする様々な転写因子が存在します4。
E-Cadherinの発現を抑制する因子には、SNAIL、SLUG、ZEB1などがあります。転写レベルで機能するこれらの抑制因子は、通常はEMT中に発現が亢進されており、EMTの開始における重要な役割を担っています。

パラフィン包埋ヒト結腸がん組織を、リコンビナントモノクローナル抗体ZEB1 (E2G6Y) XP® Rabbit mAb #70512を用いてIHCで解析しました。
塩基性ヘリックスループヘリックス (BHLH) 構造を持つ転写因子であるTWISTも、E-cadherinの発現を抑制し、間葉表現型への移行の促進に寄与します4。
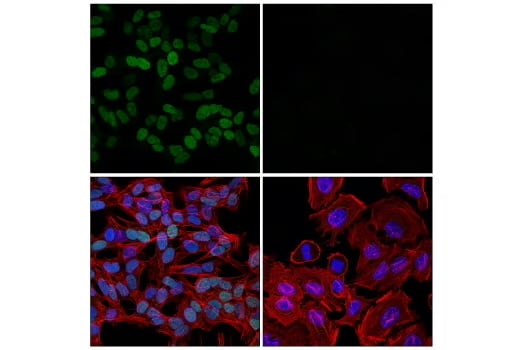
SH-SY5Y細胞 (左、ポジティブ) とHeLa細胞 (右、ネガティブ) を、リコンビナントモノクローナル抗体 TWIST1 (E5G9Y) Rabbit mAb #90445 (緑)、DyLight™ 650 Phalloidin #12956 (赤)、DAPI #4083 (青) を用いて免疫蛍光染色して解析しました。
Oct-4やNanogなどの因子も、幹細胞様の特性を誘導することによりEMTを促進します。これにより、がん細胞は急速に自己複製し、効率的に転移できるようになります。
4. EMTを誘導するシグナル伝達タンパク質
EMTの誘導には、多くのシグナル伝達タンパク質も関与しています。
その中の1つに、DDR2があります。このタンパク質は、受容体チロシンキナーゼであり、細胞外マトリックスのコラーゲンへの結合により活性化されて、様々なEMTマーカーの発現を増加させるといった遺伝子制御の変化を引き起こします。DDR2をサイレンシングすると、多くのEMTマーカーの発現が抑制されます5。
Beta-Cateninもまた、特にEMTを刺激するWntシグナル伝達経路において重要な役割を担っています6。

パラフィン包埋ヒト前立がん組織を、リコンビナントモノクローナル抗体ß-Catenin (D10A8) XP® Rabbit mAb #8480を用いてIHCで解析しました。
その他にも、通常は免疫応答に関連している細胞接着分子CD31/PECAM1も、EMTに寄与します。このタンパク質は、血管新生に関与しており、腫瘍の血管形成を可能にしてEMTを促進します。 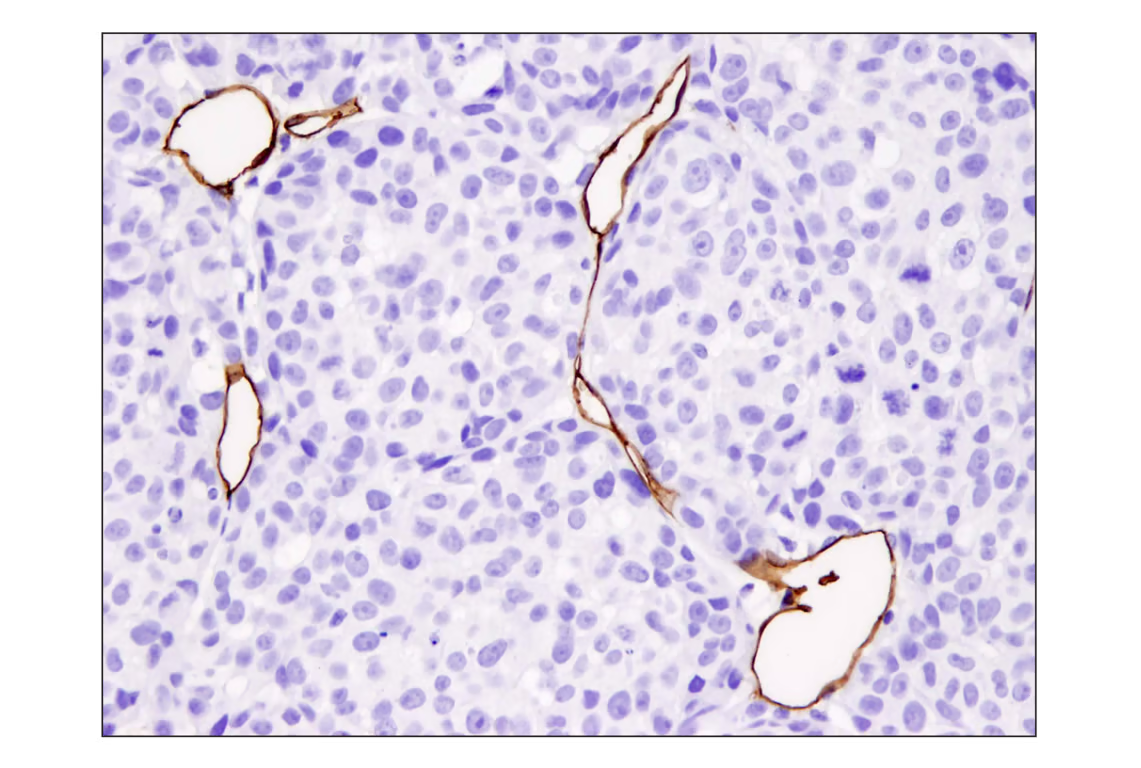
パラフィン包埋A2058異種移植片組織を、リコンビナントモノクローナル抗体CD31 (PECAM-1) (D8V9E) XP® Rabbit mAbを用いてIHCで解析しました。
がん研究における有望な標的
がんに関連する死因の約90%は、転移によるものです5。 転移がどのようにし、そしてなぜ生じるのかをより明確に理解することは、がん患者の予後を向上させるために不可欠です。
本ブログ記事で紹介したどのマーカーも、転移の重要なドライバーであるEMTがどこで生じているかを特定するのに役立ちます。がんの早期発見やより効果的な治療法につながるツールを開発するには、これらのマーカーの挙動や相互作用を研究する必要があります。
EMTの根底にあるメカニズムを完全に理解するには、より多くの研究が必要です。新たな発見があるたびに、早期介入と長期的な予後の向上が可能になり、最終的には患者の生存率とQOLの両方が改善されます。
EMT標的 |
CST製品 |
アプリケーション |
交差性 |
| Samplerキット | Epithelial-Mesenchymal Transition (EMT) Antibody Sampler Kit #9782 | 製品により異なる | 製品により異なる |
| Samplerキット | Epithelial-Mesenchymal Transition (EMT) IF Antibody Sampler Kit #49398 | 製品により異なる | 製品により異なる |
| Samplerキット | β-Catenin Antibody Sampler Kit #2951 | 製品により異なる | 製品により異なる |
| α-Smooth Muscle Actin | α-Smooth Muscle Actin (1A4) Mouse mAb (IHC Formulated) #56856 | WB, IP, IHC | H, M, R, Hm |
| α-Smooth Muscle Actin | α-Smooth Muscle Actin (D4K9N) XP® Rabbit mAb #19245 | WB, IP, IHC, IF | H, M, R, Hm, Mk |
| β-Catenin | β-Catenin (D10A8) XP® Rabbit mAb #8480 | WB, IP, IHC, IF, F, ChIP, C&R | H, M, R, Mk |
| β-Catenin | β-Catenin (15B8) Mouse mAb #37447 | WB, IHC, IF | H, M, R |
| Non-phospho β-Catenin | Non-phospho (Active) β-Catenin (Ser33/37/ Thr41) (D13A1) Rabbit mAb #8814 | WB, IP, IHC, IF, F, ChIP, C&R | H, M, R, Mk |
| CD31 (PECAM-1) |
CD31 (PECAM-1) (D8V9E) XP® Rabbit mAb #77699 | WB, IHC | M |
| CD31 (PECAM-1) |
CD31 (PECAM-1) (89C2) Mouse mAb #3528 | WB, IP, IHC, IF | H |
| CD31 (PECAM-1) |
CD31 (PECAM-1) (F2N3M) Rabbit mAb #15585 | WB, IF, F | M, R |
| DDR2 | DDR2 (E6V2N) Rabbit mAb #25814 | WB, IF | H, M, R |
| E-Catenin | E-Cadherin (24E10) Rabbit mAb #3195 | WB, IHC, IF, F | H, M |
| EpCAM | EpCAM (D4K8R) XP® Rabbit mAb #36746 | IP, IF, F | H, M, R, Hm |
| EpCAM | EpCAM (E6V8Y) XP® Rabbit mAb #93790 | WB, IP, IHC | H, M, R, Hm |
| EpCAM | EpCAM (VU1D9) Mouse mAb #2929 | WB, IHC, IF, F | H |
| Fibronectin | Fibronectin/FN1 (E5H6X) Rabbit mAb #26836 | WB, IP, IHC, IF | H |
| N-Cadherin | N-Cadherin (13A9) Mouse mAb #14215 | WB, IF, ChIP | H, M, R, Mk |
| N-Cadherin | N-Cadherin (D4R1H) XP® Rabbit mAb #13116 | WB, IP, IHC, IF | H, M |
| Nanog | Nanog (D2A3) XP® Rabbit mAb #8822 | WB, IP, IF, F, ChIP, C&R | M |
| Nanog | Nanog (D73G4) XP® Rabbit mAb #4903 | WB, IHC, IF, F | H |
| Occludin | Occludin (E6B4R) Rabbit mAb #91131 | WB, IP, IHC, IF | H, M, R |
| Oct-4A | Oct-4A (C30A3) Rabbit mAb #2840 | WB, IF, F | H, M |
| SLUG | Slug (C19G7) Rabbit mAb #9585 | WB, IP, IF, F | H, M |
| SNAIL | Snail (C15D3) Rabbit mAb #3879 | WB, IP | H, M, R, Mk |
| TWIST1 | TWIST1 (E5G9Y) Rabbit mAb #90445 | WB, IF | H, M |
| Vimentin | Vimentin (D21H3) XP® Rabbit mAb #5741 | WB, IHC, IF, F | H, M, R, Mk, Hm |
| ZEB1 | ZEB1 (E2G6Y) XP® Rabbit mAb #70512 | WB, IP, IHC, IF, F | H, M, R |
| ZO-1 | ZO-1 (D6L1E) Rabbit mAb #13663 | WB, IP, IF | H, Mk |
参考文献
- Nisticò P, Bissell MJ, Radisky DC. Epithelial-mesenchymal transition: general principles and pathological relevance with special emphasis on the role of matrix metalloproteinases. Cold Spring Harb Perspect Biol. 2012;4(2):a011908.
- Loh CY, Chai JY, Tang TF, Wong WF, Sethi G, Shanmugam MK, Chong PP, Looi CY. The E-Cadherin and N-Cadherin Switch in Epithelial-to-Mesenchymal Transition: Signaling, Therapeutic Implications, and Challenges. Cells. 2019;8(10):1118.
- Sousa AM, Liu T, Guevara O, Stevens J, Fanburg BL, Gaestel M, Toksoz D, Kayyali US. Smooth muscle alpha-actin expression and myofibroblast differentiation by TGFbeta are dependent upon MK2. J Cell Biochem. 2007;100(6):1581-1592.
- Debnath P, Huirem RS, Dutta P, Palchaudhuri S. Epithelial-mesenchymal transition and its transcription factors. Biosci Rep. 2022;42(1):BSR20211164.
- Kim D, You E, Jeong J, et al. DDR2 controls the epithelial-mesenchymal-transition-related gene expression via c-Myb acetylation upon matrix stiffening. Sci Rep. 2017;7:6847.
- Xue W, Yang L, Chen C, Ashrafizadeh M, Tian Y, Sun R. Wnt/β-catenin-driven EMT regulation in human cancers. Cell Mol Life Sci. 2024;81(1):79.

 パラフィン包埋ヒト胃がん組織を、リコンビナントモノクローナル抗体
パラフィン包埋ヒト胃がん組織を、リコンビナントモノクローナル抗体