がん研究者は近年、細胞外マトリックス (ECM) と、がんの増殖や拡散におけるその役割にますます注目しています。さらに、がん細胞だけでなくその周辺の環境、特にECM内において何が起こっているのかに着目した治療法の開発への関心が高まっています。
ECMは、タンパク質やその他の分子のネットワークで構成されており、組織の構造を形成し、細胞の秩序の維持をサポートします。しかし、ただ単に物理的な枠組みを提供しているだけでなく、増殖や運動、生存、分化といった重要な細胞プロセスを調節する役割も担っています。
がん微小環境 (TME) におけるECMは、その役割が大きく変化しています。この再構築されたECMは、免疫環境を弱体化させて、がん化した細胞を自然免疫応答から保護することがあります。また、このECMの変化は、がんにとって増殖および拡散するための理想的な状況を作り出し、薬物の送達を阻害して治療抵抗性に寄与することにより、がんの治療を困難にしている可能性があります。ECMに対する理解が深まるにつれ、ECMそのものが治療標的になりうるとの見方が強まっています。現在、ECMの特定の部位を標的とし、その挙動に影響を与えて、腫瘍の保護ではなく抗腫瘍効果を示すようにECMを変化させる方法が探索されています。
|
|
関連するCST Antibody Samplerキットを探索してください。キットには、本ブログで紹介する多くのマーカーに対する試薬が含まれます。 |
|
まず、腫瘍の増殖をサポートする構造タンパク質や腫瘍の進行に関連するシグナル伝達タンパク質、TMEの再構築を促すECM修飾タンパク質などの、治療標的となる可能性が高い主なECMマーカーをいくつか紹介します。
<Jump to the product list at the end of this post>
構造タンパク質:ECMの基本的な要素
構造タンパク質は、ECMの骨組みとなります。これらのタンパク質は、組織の構築やその完全性の維持をサポートしますが、がんにおいては、腫瘍の増殖と治療抵抗性をサポートします。
- Collagenは、ECMの約90%を占めています1。正常組織に不可欠なタンパク質ですが、腫瘍においてその濃度が高い場合は、予後不良となることが多々あります。がん細胞の増殖や拡散、治療抵抗性をサポートします2。Collagenの主なマーカーには、COL1A1やCOL11A1、COL6Aなどがあります。
/66948_IHC%20analysis%20using%20COL1A1%20monoclonal%20antibody_small.png?width=507&height=316&name=66948_IHC%20analysis%20using%20COL1A1%20monoclonal%20antibody_small.png)
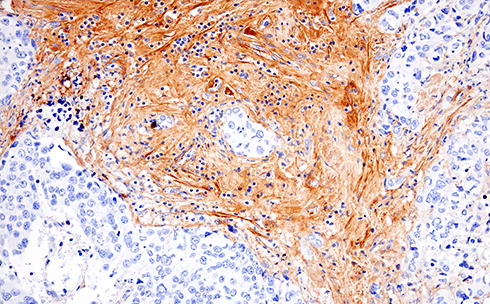
パラフィン包埋ヒト非小細胞肺がんを、モノクローナル抗体COL1A1 (E3E1X) Mouse mAb #66948を用いてIHCで解析しました。
- Lamininは、細胞基底膜を構成する重要なタンパク質です1。このタンパク質は、がん化した細胞の接着や全身への遊走、他の組織への浸潤を可能にし、がんの転移を促す重要な役割を担っています3。 Lamininは、alpha (LAMA)、beta (LAMB)、gamma (LAMC) といった3種類の異なるポリペプチド鎖で構成されています。
/53884_LAMC2_ECM%20TME%20marker_A-431%20cells.png?width=507&height=252&name=53884_LAMC2_ECM%20TME%20marker_A-431%20cells.png)
A-431細胞 (ヒト類表皮がんの細胞株モデル) を、リコンビナントモノクローナル抗体LAMC2 (E9F7M) Rabbit mAb #53884 (緑)、DyLight™ 554 Phalloidin #13054 (赤)、DAPI #4083 (青) を用いてIFで解析しました。
- Elastinは通常、組織に柔軟性と弾力を与えます。しかし、このタンパク質が分解されると、腫瘍の発達を促進するエラスチン由来ペプチド (EDP) が生成されます1,4。
腫瘍促進性タンパク質:増殖と拡散の促進
ECMタンパク質の中には、腫瘍の構造を支えるだけでなく、発達を積極的に促すものもあります。以下で紹介するマーカーは、浸潤性や転移性、治療抵抗性の向上と関連しています。
- Fibronectinは、がん細胞の増殖と拡散をサポートすることが分かっています。このタンパク質は、上皮間葉転換 (EMT) 中に発現量が上昇し、腫瘍の浸潤や転移の増加に関与しています。そのため、Fibronectinの発現が高い場合は、がん細胞が間葉系へと変化している可能性があります。
/26836_IHC%20analysis%20using%20Fibronectin%20antibody%20in%20breast%20cancer.png?width=490&height=304&name=26836_IHC%20analysis%20using%20Fibronectin%20antibody%20in%20breast%20cancer.png)
パラフィン包埋ヒト乳管がん組織を、リコンビナントモノクローナル抗体Fibronectin/FN1 (E5H6X) Rabbit mAb #26836を用いてIHCで解析しました。
- Tenascin-Cは、TME内の細胞の遊走を促進します。また、腫瘍の浸潤に不可欠であるとする研究もあります5。腫瘍間質の構成要素であるこのタンパク質は、しばしば悪性度の高いがんで高発現しています。
- Thrombopondin-1は、細胞の接着や遊走、アポトーシス、炎症、血管機能、がんの発達を制御するECMタンパク質です。また、このタンパク質は、新しい血管形成 (血管新生) を阻害することにより、腫瘍の発達を遅らせる能力を持つ可能性があります6。
/37879_WB%20analysis%20thrombospodin-1%20antibody.jpeg?width=520&height=350&name=37879_WB%20analysis%20thrombospodin-1%20antibody.jpeg)
上皮細胞や上皮様細胞、線維芽細胞の様々な細胞株 (ACHN、ScaBER、LN18、mIMCD-3、MEF) からの抽出物を、Thrombospondin-1 (D7E5F) Rabbit mAb #37879を用いてウェスタンブロットで解析しました。
- Osteopontin (OPN) は、細胞の接着や遊走に関与していると考えられており、近年改めて、腫瘍の転移を促進することが示されています。また、このタンパク質は、腫瘍形成にも関与しています。腫瘍形成とは、正常な細胞ががん細胞に変化し、疾患がさらに進行する過程を指します7。治療の標的となる可能性を秘めており、現在研究が進められています8。
/88742_IHC%20analysis%20using%20osteopntin%20SPP1%20antibody.jpg?width=501&height=311&name=88742_IHC%20analysis%20using%20osteopntin%20SPP1%20antibody.jpg)
パラフィン包埋マウス卵巣組織を、リコンビナントモノクローナル抗体Osteopontin/SPP1 (E9Z1D) Rabbit mAb #88742を用いてIHCで解析しました。
ECM修飾タンパク質:がん微小環境の再構築
最後に紹介するECM修飾タンパク質は、ECMを、がん化した細胞の拡散に寄与するように変化させます。
- Hyaluronanは、ECMに存在するGAG (Glycosaminoglycan) の一種であり、腫瘍細胞の増殖やアポトーシス、血管新生、転移に影響を及ぼします。このタンパク質は、TMEにおいてバリアを形成し、薬物の腫瘍部位への送達を阻害します9。
/53721_IHC%20analysis%20hyaluronan%20staining%20kit.jpg?width=500&height=336&name=53721_IHC%20analysis%20hyaluronan%20staining%20kit.jpg)
パラフィン包埋ヒト大腸がん組織を、Hyaluronan Complete Tissue Staining Kit (Alexa Fluor® 488) #53721 (緑) およびDAPI #4083 (青) で染色し、IHCで解析しました。
- Lysyl oxidase (LOX) は、CollagenとElastin間の架橋形成に関与する酵素です。このタンパク質は、ECMを強化することにより腫瘍の発達を促進します。
- MMP (Matrix metalloproteinase) ファミリーのMMP-2、MMP-9、MMP-1、MMP-14 (MT1-MMP) は、ECMの構成要素を分解する酵素であり、がん細胞の拡散を容易にします。
/13667_WB%20analysis%20of%20MMP9%20antibody.jpeg?width=520&height=350&name=13667_WB%20analysis%20of%20MMP9%20antibody.jpeg)
未処理のU-2 OS細胞 (-)、もしくはTPA #4174で処理 (200 μM、48時間) したU-2 OS細胞 (+) からの抽出物と、濃縮したこれらの細胞の培養液を、リコンビナントモノクローナル抗体MMP-9 (D6O3H) XP® Rabbit mAb #13667を用いてウェスタンブロットで解析しました。予想通り、MMP-9はTPA処理により誘導されました。
- Versicanは、CSPG (Chondroitin sulfate proteoglycan) であり、ECMの構成要素と相互作用して、がん細胞の増殖や生存、血管新生、浸潤、転移を促進します。
- Peropstinは、損傷に応答したECMリモデリングに関与する基質タンパク質であり、細胞の増殖や生存、接着、ひいてはがん細胞の転移を引き起こす可能性があります。
がん研究において細胞外マトリックスが注目される理由
これらのマーカーは、がん研究分野が拡大するにつれ、次世代のがん治療の開発における重要な役割を担う可能性があります。
研究者は、これらのタンパク質に固有の特性と、がんの発達におけるECMの役割をより深く理解することにより、新たな治療戦略を見出したいと考えています。
参考文献
- Huang J, Zhang L, Wan D, et al. Extracellular matrix and its therapeutic potential for cancer treatment. Signal Transduct Target Ther. 2021;6(1):153. Published 2021 Apr 23. doi:10.1038/s41392-021-00544-0
- Fang M, Yuan J, Peng C, Li Y. Collagen as a double-edged sword in tumor progression. Tumour Biol. 2014;35(4):2871-2882. doi:10.1007/s13277-013-1511-7
- Aleman JD, Young CD, Karam SD, Wang XJ. Revisiting laminin and extracellular matrix remodeling in metastatic squamous cell carcinoma: What have we learned after more than four decades of research?. Mol Carcinog. 2023;62(1):5-23. doi:10.1002/mc.23417
-
Wang Y, Song EC, Resnick MB. Elastin in the Tumor Microenvironment. Adv Exp Med Biol. 2020;1272:1-16. doi:10.1007/978-3-030-48457-6_1
- Sun Z, Schwenzer A, Rupp T, et al. Tenascin-C Promotes Tumor Cell Migration and Metastasis through Integrin α9β1-Mediated YAP Inhibition. Cancer Res. 2018;78(4):950-961. doi:10.1158/0008-5472.CAN-17-1597
- Ming-Ping Wu, Li-Wha Wu, Cheng-Yang Chou (2016) The anticancer potential of thrombospondin-1 by inhibiting angiogenesis and stroma reaction during cervical carcinogenesis, Gynecology and Minimally Invasive Therapy, Volume 5: 2, 48-53
- Zhao H, Chen Q, Alam A, et al. The role of osteopontin in the progression of solid organ tumor. Cell Death Dis. 2018;9(3):356. Published 2018 Mar 2. doi:10.1038/s41419-018-0391-6
- Bandopadhyay M, Bulbule A, Butti R, et al. Osteopontin as a therapeutic target for cancer. Expert Opin Ther Targets. 2014;18(8):883-895. doi:10.1517/14728222.2014.925447
- Zhao J, Chen J, Li C, Xiang H, Miao X. Hyaluronidase overcomes the extracellular matrix barrier to enhance local drug delivery. Eur J Pharm Biopharm. 2024;203:114474. doi:10.1016/j.ejpb.2024.114474


/26836_IHC%20analysis%20using%20Fibronectin%20antibody_thumbnail.jpeg?width=117&height=153&name=26836_IHC%20analysis%20using%20Fibronectin%20antibody_thumbnail.jpeg)