ヒトの体内にある膨大な量のDNAには、本当に当惑させられます。体細胞1個に由来するDNAは、端から端まで伸ばすと約2メートルの長さとなり、平均的な人のDNAすべてを引き伸ばすと、その長さは太陽系の端まで到達してから戻ってくることができるほどです!
ヒトのゲノムは30億塩基対のDNAから成り、環境の変化や体内の変化に対応するには、これらすべてを読み取り、解読し、タンパク質に翻訳する必要があります。このプロセスを体系化するため、DNAはクロマチンにコンパクト化されています。DNAはコアヒストン8量体に巻き付いてヌクレオソームを形成しており、このヌクレオソームはその後、さらに折りたたまれて高次のクロマチン線維にコンパクト化される場合もあります。コンパクト化されると、きつく巻き付いたクロマチンは、多様なタンパク質複合体とヒストン修飾により開かれてユークロマチンにならない限り、転写されることはできなくなります。ATP依存性クロマチンリモデラーはここで役割を果たします。
ATP依存性クロマチンリモデラーは、ATP加水分解に依存してヌクレオソームを除去し、転写因子がアクセス可能になります。この機能は複数のタンパク質複合体が果たしていますが、最近の研究でBAF (Brahma associated factor) と呼ばれるタンパク質群について、がんにおける変異の発生率が特に高くなることが明らかにされています。BAF複合体は古くから研究されていますが、オミクス技術とビッグデータ解析の発展により、これらのクロマチンリモデラーががんや疾患おける重要な役割が、ようやく明らかになり始めています。実際に、ヒトのがん約4症例につき1症例において、BAF複合体構成因子に変異が見つかっています (1)。
しかし、腫瘍におけるBAF変異の保有率がこれほどに高いのはなぜなのでしょうか?この質問に対する答えは、この複合体そのものと同様に複雑です。多数のBAFタンパク質ががん抑制因子として機能し、その変異が、ラブドイド腫瘍 (BAF47発現なし) や卵巣明細胞腫瘍 (ARID1A発現なし) などの、浸潤性の高いタイプのがんの原因になることが分かっています (2,3)。ラブドイド腫瘍は、特に変異が非常に少ない腫瘍であり、BAF47遺伝子は、ラブドイド腫瘍で変異のみられるわずかな遺伝子の一つです。
他の例では、BAF複合体の構成因子が、がんの促進因子となっていることが知られています。髄液肉腫は、BAFを構成するSS18のN末端と、SSX1、SSX2、SSX4タンパク質のC末端との発がん性融合によって促進される、稀少なタイプの腫瘍です。SS18/SSXがんタンパクがBAFに取り込まれると、野生型BAF47は排除され、複合体を実質的に乗っ取りゲノムの別の部分に移動させ、Sox2 などの発がん性因子を発現させます (4,5)。こうしたBAF複合体による発がん性の「乗っ取り」は、TMPRSS2-ERG融合を含む前立腺がんでも確認されてきています (6)。
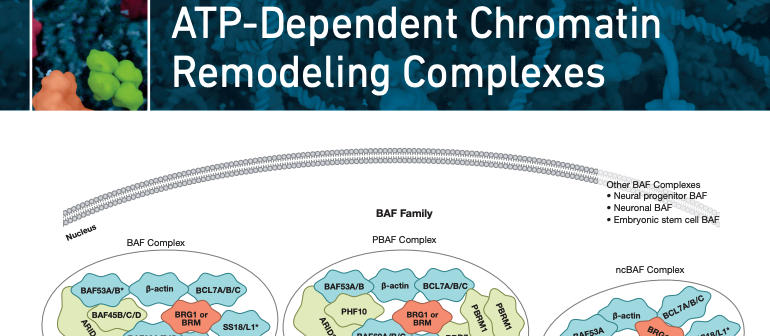
このような多様なサブユニットがどのように発がんに寄与しているかを真に理解するには、BAX複合体の微細な制御機構を理解する必要があります。ごく最近までBAF複合体がどのように形成されるかだけでなく、その構成因子の正体すら、ほとんど知られていませんでした。現在は、25以上の異なるサブユニットから成り、その多くが3つの異なる複合体を構成する相互排他的なホモログであることが分かっています。それぞれの複合体は、BAF60ホモログがBAF155/170ホモまたはヘテロ二量体に加わることで形成が始まります。そこから、可変サブユニットが、標準的 (BAF)、非標準的 (ncBAF)、または、BAF180/PBRM1を含むBAF (PBAF) 複合体に取り込まれます。各複合体はゲノム内の異なるスペースを占拠するため、いずれも固有の機能を持っていると考えられます。
3つの主要な複合体に加え、組織/細胞種に特異的なBAF複合体もあります。神経前駆細胞が有糸分裂後ニューロンに分化するにつれ、サブユニットは交換され神経特異的BAF複合体 (nBAF) を形成します (7)。nBAFは正常な脳機能で重要な役割を果たし、その様々な構成因子の変異は、コフィン・シリス症候群などの発達障害を引き起こすことがあります (8~10)。胚性幹細胞 (ES細胞) にもesBAFと呼ばれる特異的なBAFのバリアントがありますが、これは、自己複製能と多分化能に必要不可欠です (11,12)。
BAF複合体の基本的な生物学的特性に関する知見が得られて、以前は治療不可能だったタイプの腫瘍について、重要な発見がなされてきています。例えば、固有のncBAF構成因子であるBRD9が同定され、このBRD9が、ラブドイド腫瘍と髄液肉腫において最も変異が頻発する部位であることが分かってきました (13, 14)。
実際に、合成致死性の探索が、急速にBAF研究の対象領域となりつつあります。腫瘍は、相互排他的なホモログの機能性構成因子(Brg1/BRMやARID1A/Bなど)1つを必要とすると考えられます (15,16)。BAF変異腫瘍では、PRC2の構成因子であるEzh2など、非BAF関連タンパク質の関与も認められます (17)。Ezh2や BET阻害剤はすでに広く利用可能であり、 BAF変異を伴うがんに対して、併用療法の開発も期待されています。
ヒトの細胞内にある膨大な量のDNAには、実際に当惑させられますが、最近の相次ぐ研究により、細胞がDNAをどのように管理しているかが判明し始め、また病態に対する理解や治療法も進歩しています。
関連経路を調べる。
参考文献:
- 23644491
- 9671307
- 20826764
- 23540691
- 29861296
- 30078722
- 17640523
- 28824374
- 22426308
- 22426309
- 19279218
- 19279220
- 30397315
- 31015438
- 24520176
- 24562383
- 26552009