このほど、クローン病 (CD) を患う小児患者の複雑なマイクロバイオームを解き明かし始める、オタワ大学Daniel Figeys研究室の新しい研究がNature Communicationsに発表されました。これは炎症性腸疾患 (IBD) の1種で、消化管に炎症を引き起こし、腹痛、激しい下痢、疲労、体重減少、栄養失調などの症状を引き起こします。
この疾患には、免疫系、遺伝的要因、環境的要因など、様々な要因が関与していますが、腸内細菌叢 (gut microbiome) もその一因となっています。主要なアミノ酸の翻訳後修飾は、CDでどのような役割を果たしているのでしょうか?
これを解明するため、Figeys研究室はCD小児患者群と健常小児群のリジンのアセチル化の違いを調べる研究をデザインしました。
リジン残基のアセチル化は、原核生物を含む全生命界で広くみられますが、本研究は小児CDにおけるリジンのアセチル化 (Kac) とマイクロバイオームの関係を検討した初めての研究です。リジンのアセチル化はタンパク質の重要な翻訳後修飾 (PTM) で、走化性、栄養代謝、ストレス応答など、多くの生物学的プロセスを制御することが知られています。しかし、マイクロバイオームは複雑であり、またKac部位をもつペプチドの濃縮は困難であることなどから、マイクロバイオームにおけるKac部位のグローバルな解析は行われていませんでした。
筆者らはCell Signaling Technology (CST) のAcetylated-Lysine Antibodyを用いて、患者の腸管粘膜由来のKacペプチドを濃縮し、質量分析と強力なインフォマティクスのパイプラインを組み合わせて、ヒトや微生物のタンパク質の35,000以上のKacペプチドを同定しました。詳細な定性解析と定量解析により、CD患者とコントロールの間で、52の宿主Kac部位と136の微生物Kac部位の存在量に差があることが分かりました。このデータから、CD患者で減少した部位の大半は、短鎖脂肪酸 (SCFA) の産生に重要なFirmicutes属の細菌に由来することが分かりました。このデータは、CD患者のFirmicutesのレベルはコントロールと比較して低下すると言う知見を裏付けています。
リジン脱アセチル化酵素 (KDAC) 阻害剤がCDの治療に有効であることが知られていますが、この結果からKDACの有効性の一部は、腸内細菌叢との相互作用によることが示唆されました。さらに、患者のプロテオームにおいて、CD患者とコントロールの間で、免疫応答に関与するいくつかのKac部位の存在量に差があることが分かりました。この研究は、マイクロバイオームを解明するための新たな手がかりと、CDの新たな研究を発展させるためのロードマップを提供しています。
CSTは、この研究においてFigeys研究室をサポートできたことを大変嬉しく思います。LC-MS/MS解析のためのアセチル化リジンペプチドの濃縮の詳細は、PTMScan® Acetyl-Lysine Motif [Ac-K] KitおよびCSTプロテオミクス解析サービスをご覧ください。
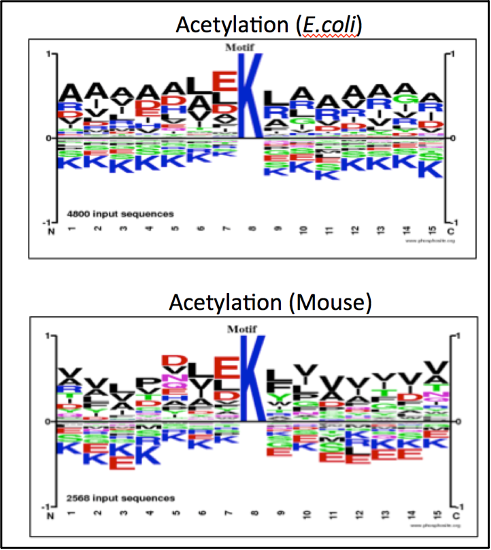
AcetylScan®アッセイのデータ。PhosphoSitePlus®のSite Logo Generatorを使用して修飾されたリジン残基周辺のモチーフを検索した非冗長なペプチド配列を示しました。大腸菌KacペプチドはMG1655株から、マウスアセチル化ペプチドはBalb-Cマウス肝臓組織から得られました。
AcetylScan、Cell Signaling Technology、CST、PhosphoSitePlus、PTMScanはCell Signaling Technology, Inc.の登録商標です