CST®抗CARリンカー抗体は、2023年のCiteAb Innovation Awardを受賞しました。その理由をご覧ください!
—
キメラ抗原受容体 (CAR) T細胞療法とは、生体内の自身の免疫系を活用して抗腫瘍効果を誘導する、画期的かつ急速に進化している養子細胞免疫療法であり、大きな期待が寄せられています。新しいCAR-T療法の開発において、細胞表面に発現するCARの特性解析用の検出試薬は、新しい治療法の検証や最適化に不可欠です。
しかしながら、新規腫瘍抗原に対する新たなCARをデザインした場合、CARの細胞表面の発現を確認するための独自の検出試薬を開発し、その都度検証する必要があります。このプロセスは、コストと時間がかかるだけでなく、非特異的な検出による問題を引き起こし、開発のさらなる遅延につながります。
では、抗原の特異性に関係なく、CARの同定および発現を確認できる汎用性の高い検出試薬があるとしたらどうでしょうか?CSTは、改変された免疫細胞上に発現する幅広いCARを認識できるように設計された検出試薬のパネルを開発しました:それが抗CARリンカー抗体です。
市場初となるこれらの試薬は、複数のパラメーターを検出するフローサイトメトリーパネルに組み込むことが可能であり、非臨床モデルにおけるCARの発現や輸送、持続性をモニタリングできます。
<<標識抗体などを含む、弊社のCARリンカー製品をご覧ください>>
現在のアプローチ:フローサイトメトリーを用いた細胞表面のCARの検出
この新しいCAR検出技術の仕組みを理解するために、まずはCAR-T細胞の構造と機能を紹介します。
CARは、T細胞応答を調節して自己由来の腫瘍抗原を攻撃するように再設計された、改変型受容体です。その名の通り、この受容体は4つの主な構成因子からなるキメラタンパク質であり、細胞外標的抗原結合ドメイン (単鎖可変領域フラグメントまたはscFvなど) 、スペーサーまたはヒンジドメイン、膜貫通ドメイン、細胞内シグナル伝達ドメイン (少なくとも1つは含む) に分けられます (図1)。これらの要素をうまく組み合わせることにより、CAR-T細胞は目的の抗原を認識し、腫瘍細胞を殺すことができるようになります1。
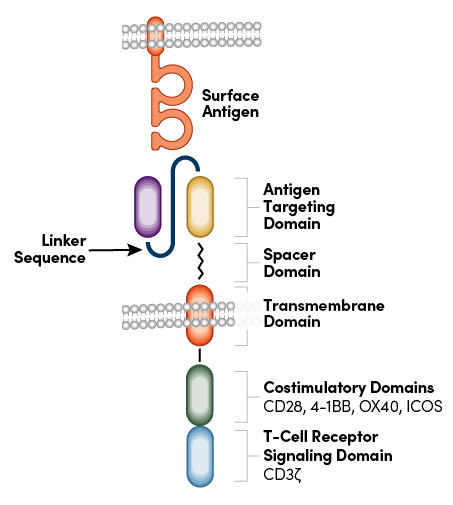 図1:CARの構造の詳細:抗原を標的化するドメインやリンカー配列など
図1:CARの構造の詳細:抗原を標的化するドメインやリンカー配列など
科学者は、創薬や非臨床研究においてCAR-T細胞を設計する際に、フローサイトメトリーを使って細胞表面のCARの発現をモニタリングし、CAR-T細胞が機能していることを確認する必要があります。
現在は、scFvの重鎖可変ドメインや軽鎖可変ドメイン、またはヒンジドメイン内の特定の配列を認識する試薬を用いて、CARの細胞外ドメインを検出する方法が主流です。
使用するCAR-T検出試薬によっては、使用可能なソリューションでの特異性に欠ける、フローサイトメトリーパネルに組み込みにくい、単一のCARの検出にしか使えない、などの問題が生じます。
抗CARリンカー抗体とは何か?どのように機能するのか?
CST抗CARリンカー抗体は、重鎖可変ドメインや軽鎖可変ドメイン、ヒンジドメイン内の配列を標的とする代わりに、scFvの重鎖可変ドメインと軽鎖可変ドメインの間にあるリンカー配列を標的とします。scFvをベースに設計されるCARのほとんどが、グリシン - セリンリンカー (G4Sリンカー) 配列の繰り返し、またはWhitlow抗体のいずれかを含むため2、抗G4S抗体および抗Whitlowモノクローナル抗体を用いれば、scFvをベースとするあらゆるCARの細胞表面の発現をフローサイトメトリーでモニタリングできます (図2)。
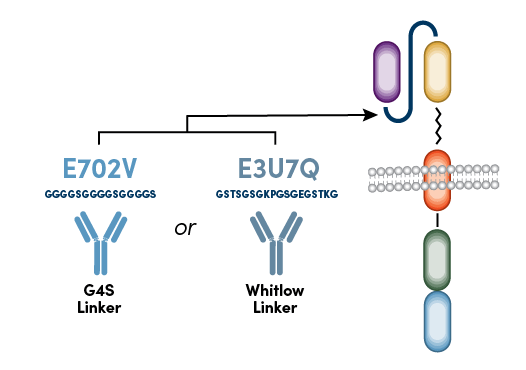
図2:CST抗CARリンカー抗体が認識する、G4Sリンカー配列またはWhitlowリンカー配列
B細胞悪性腫瘍で高発現がみられる細胞表面分子のCD19抗原とCD20抗原を標的とするCARなど、あらゆるCARにこのリンカー配列が含まれています。
 ヒトPBMCから単離し、G4Sリンカーを含むscFvベースの抗CD20 CARを発現するように改変した汎CD3陽性T細胞を、G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907 (右) または同じ濃度のRabbit (DA1E) mAB IgG XP Isotype Control PE Conjugate #5742 (左) を用いてライブセルフローサイトメトリーで解析しました。 TagBFP (Tag Blue fluorescent protein) はCARと共発現しています。データは、Micahel Kvrjak、Lohmueller研究室 (ピッツバーグ大学) からご提供いただきました。
ヒトPBMCから単離し、G4Sリンカーを含むscFvベースの抗CD20 CARを発現するように改変した汎CD3陽性T細胞を、G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907 (右) または同じ濃度のRabbit (DA1E) mAB IgG XP Isotype Control PE Conjugate #5742 (左) を用いてライブセルフローサイトメトリーで解析しました。 TagBFP (Tag Blue fluorescent protein) はCARと共発現しています。データは、Micahel Kvrjak、Lohmueller研究室 (ピッツバーグ大学) からご提供いただきました。
これらの抗体は、すべてのCST製品と同様に、Hallmarks of Antibody Validation (抗体検証における戦略) に従ってアプリケーションごとに厳密に検証されています。これらの検証には、異なる腫瘍抗原を認識するCARを発現する初代ヒトT細胞など、関連するモデル系での試験も含まれます。弊社は、3種類の異なる標識抗体を提供しています。また、CSTのカスタム標識サービスを利用して、カスタム標識することもできます。
 汎用性の高い、検証済みCAR検出試薬を用いることにより、不必要で時間のかかるステップを省き、探索研究または医薬品開発のプロセスを加速することができます。
汎用性の高い、検証済みCAR検出試薬を用いることにより、不必要で時間のかかるステップを省き、探索研究または医薬品開発のプロセスを加速することができます。
下の表では、抗CARリンカー標識抗体と組成の一部を紹介していますが、常に多くの製品が追加されています。CARリンカーのマッチド抗体ペアやCAR Cell Enrichmentキットなどを含む、弊社の拡大中の最新製品リストについては、こちらをご覧ください。さらに、CAR-T細胞の表現型解析用の蛍光色素標識抗体や、組織中のCAR標的を解析するための様々なIHC検証済みモノクローナル抗体も提供しています。
CAR-T療法の迅速な開発
生体内の自分の免疫系を抗がん治療に使用することは、がん研究者たちの長年の夢でしたが、CAR-T療法によりその夢が現実のものとなりました。CAR-T療法は「Living Drug (生きた薬)」と呼ばれ、1回の投与で数十年にわたる治療効果が得られます。
「この画期的な新製品であるCST抗CARリンカー抗体は、がん患者に大きな影響を与え、新たな治療法の開発や最適化に役立つ可能性があります。」- CiteAb 2023 Innovation Awards
この画期的な治療法を用いた血液悪性腫瘍の治療が成功したことにより、主に固形がんや線維性肝疾患、糖尿病などの老化関連疾患における新たな治療法の開発への道が開かれました3-5。この非常に有望な治療法は、いまだ免疫療法の最前線にありますが、現在開発中の新しい治療法が、これまで選択肢が限られていたり、治療が困難であったがん患者にとって革新的なものになることは間違いありません。
詳細はこちら:
- 関連ブログ:迅速なT細胞活性化および増殖を活用して免疫腫瘍学研究を加速
- CAR-T療法の研究に役立つツールの詳細はこちらをご覧ください
- CARシグナル伝達ネットワークのインタラクティブパスウェイ図を探索してください
- CAR-T細胞の設計方法や現在の研究課題の詳細については、CAR-Tビデオシリーズをご覧ください
参考文献:
- Labanieh L, Majzner RG, Mackall CL. Programming CAR-T cells to kill cancer. Nat Biomed Eng. 2018;2(6):377-391. doi:10.1038/s41551-018-0235-9
- Whitlow M, Bell BA, Feng SL, et al. An improved linker for single-chain Fv with reduced aggregation and enhanced proteolytic stability. Protein Eng. 1993;6(8):989-995. doi:10.1093/protein/6.8.989
- Mohanty R, Chowdhury CR, Arega S, Sen P, Ganguly P, Ganguly N. CAR T cell therapy: A new era for cancer treatment (Review). Oncol Rep. 2019;42(6):2183-2195. doi:10.3892/or.2019.7335
- Li JH, Chen YY. A Fresh Approach to Targeting Aging Cells: CAR-T Cells Enhance Senolytic Specificity. Cell. 2020;27(2):192-194. doi:10.1016/j.stem.2020.07.010
- Tenspolde, M., Zimmermann, K., Weber, L. C., Hapke, M., Lieber, M., Dywicki, J., Frenzel, A., Hust, M., Galla, M., Buitrago-Molina, L. E., Manns, M. P., Jaeckel, E., & Hardtke-Wolenski, M. (2019). Regulatory T cells engineered with a novel insulin-specific chimeric antigen receptor as a candidate immunotherapy for type 1 diabetes. Journal of Autoimmun. 2019;103:102289. doi:10.1016/j.jaut.2019.05.017
CST and Cell Signaling Technology are trademarks or registered trademarks of Cell Signaling Technology, Inc. Alexa Fluor is a registered trademark of Life Technologies Corporation. All other trademarks are the property of their respective owners. Visit cellsignal.com/trademarks for more information. 22-BPA-10837