ご寄稿いただいたRichard I. Gregory博士は、ハーバード大学医学大学院の教授であり、ボストン小児病院で幹細胞プログラムの主任研究員を務めています。現在、がんにおけるエピトランスクリプトームの研究に従事しており、最新の研究では、RNAメチルトランスフェラーゼ (MTase) であるMETTL3とMETTL1を、様々ながんにおける新規がん遺伝子として特定しました。
—
細胞内RNAは、多様な化学物質で修飾されています1。 近年、特定のRNAの化学修飾部位が網羅的にマッピングされたことにより、エピトランスクリプトームが解明されつつあります2。 個々の修飾は、コーディングRNAまたは非コーディングRNA、あるいはその両方を含む様々なサブセットで発生し、RNAの生合成や安定性、局在または機能などに影響を与え、最終的には遺伝子発現の転写後調節という、現在まだ解明されていない重要な役割を果たしていると考えられています。さらに、特定のRNAの修飾を担う酵素の遺伝子変異や増幅、発現量の調節不全は、それぞれが単独または協調して、小児期における発達障害や多くのがんと関連します。
世界的なm7G RNAメチロームを解明するためのトランスクリプトームワイド関連解析
N7-メチルグアノシン (m7G) は、原核生物や真核生物、一部の古細菌に広くみられるtRNA修飾であり、特定のtRNAに含まれる可変ループ内のヌクレオチド部位G46が修飾されています。この修飾は、tRNAの機能的立体構造を安定化し、分解を防ぐのに役立ちます3。
ボストン小児病院のGregory研究室の最新の研究では、トランスクリプトーム全体におけるm7Gの包括的なマッピングに、抗体ベースおよび化学ベースのアプローチとハイスループットの相補的DNA (cDNA) シーケンシングを組み合わせて用いています。私たちは、マウス胚性幹細胞 (mESC) とヒトのがん細胞株において、一塩基レベルの分解能でm7G tRNAメチロームを特異的に解析できる、m7Gメチル化tRNA免疫沈降ーシーケンシング (m7G MeRIP-Seq) と、tRNA還元切断シーケンシング (TRAC-Seq) を開発しました4-6。これらの技術を用いた世界規模の調査により、tRNAの可変ループ領域内のRAGGUモチーフが修飾されたtRNAのサブセットを発見することができました。
これらの結果から、m7G修飾が主にtRNAに限定されていることが示唆され、この結論は関連する解析により裏付けられています7。一方、同じ頃に行われた他の研究では、特定のメッセンジャーRNA (mRNA) やマイクロRNA前駆体 (pri-miRNA) などの転写産物などにおけるm7G修飾の存在を報告していますが、これらの結果は議論の余地があり、さらなる調査が必要です8-10。
m7Gメチルトランスフェラーゼ (MTase) 複合体:METTL1/WDR4
m7G46は、哺乳動物ではMETTL1 (Methyltransferase 1) とその最も重要なコファクターであるWDR4 (WD Repeat-Containing Protein 4) により触媒されます。METTL1は、すでに酵母で同定されていたTrm8/Trm82複合体のオーソログです11。最新の構造研究により、7G MTase複合体がどのように特定のtRNA基質に特異的に結合し、修飾するかについての新たな知見が得られています12, 13。酵母複合体は、熱ストレス下での成長に必要になりますが、最適な条件下では必要ありません14。一方、METTL1とWDR4は、mESCの正常な細胞周期進行と分化に必要であり、それらの変異や調節不全はヒトの疾患につながります4, 15, 16。
METTL1/WDR4 MTase複合体の欠損は発達障害を引き起こす
ヒト染色体21q22.3に位置するWDR4遺伝子の生殖細胞変異は、顔面異形や脳形成異常、てんかん発作を伴う重症脳症を特徴とする小頭性原発性小人症にみられる異常を引き起こします15, 16。WDR4は、ヒトでは、この染色体領また、WDR4は、ヒトにおけるこの染色体領域のトリソミーを原因とする、精神遅滞を伴うダウン症候群にみられるいくつかの表現型を引き起こす候補遺伝子です17。 実際にWDR4は、ダウン症候群のモデルマウスにおける過剰発現により、学習と記憶に影響を与えることがわかっている候補遺伝子のうちの1つです18。同じ遺伝子群のモノソミーも認知や海馬の可塑性に影響を与えることから、この染色体領域内の特定の遺伝子の正確な投与量が正常な脳機能にとって重要であるという説が支持されています19。
興味深いことに、mESCのMETTL1またはWDR4のいずれかを欠損させることにより、細胞分化、特に神経系の発達時における外胚葉分化が損なわれます (図1)4。リボソームプロファイリング (Ribo-Seq) を用いた研究により、その機構として、METTL1ノックアウトESCでは、細胞周期に関連する遺伝子や前脳の形態を調節する遺伝子のmRNAの翻訳効率が低下していることや、これらのmRNAには翻訳にm7G修飾tRNAを必要とするコドンに富むことがわかっています4。
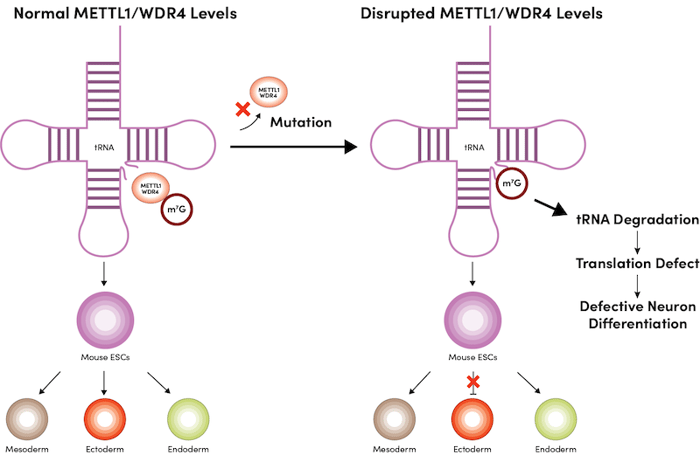
図1:マウスmESCにおけるMETTL1またはWDR4のいずれかの欠損により、神経細胞の分化が損なわれます。
mESCにおけるm7G tRNA修飾の、分子および細胞レベルでの重要性に関するこれらの結果から、ヒトの発達障害の病因に関する新たな知見が得られています。
METTL1/WDR4 MTase複合体の調節不全はがんを引き起こす
私たちは近年、ヒトの多くのがんにおいて遺伝子増幅や過剰発現がみられる新たながん遺伝子として、METTL1を同定しました6。METTL1の欠損は、いくつかの異なるがんモデルにおいて、がん細胞の増殖や細胞周期の進行だけでなく、腫瘍の成長も強く抑制します。
逆に、METTL1/WDR4複合体の過剰発現は、細胞増殖の増加や細胞周期の進行の加速、コロニー形成の促進、in vivoでの腫瘍形成など、悪性形質転換を引き起こします (図2)。
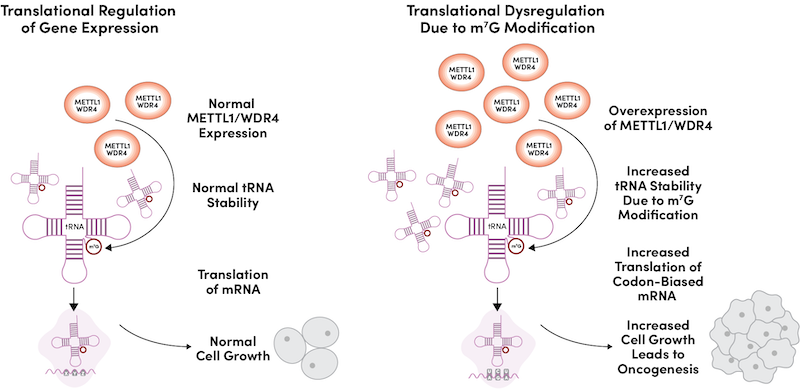 図2:MTase複合体の発現量の増加が、tRNAの安定性と発現量の増加を誘導し、細胞周期調節因子のmRNAの翻訳が増加することにより、細胞の成長と発がんの原因となります。
図2:MTase複合体の発現量の増加が、tRNAの安定性と発現量の増加を誘導し、細胞周期調節因子のmRNAの翻訳が増加することにより、細胞の成長と発がんの原因となります。
その機構として、MTase複合体の発現量の増加により、m7G修飾されたtRNAのサブセットが増え、m7G修飾されたtRNAが解読するmRNA、特に細胞周期調節因子のmRNAの翻訳とタンパク質発現が増加します6。近年、多くの異なるがんにおいてMETTL1/WDR4の発がん活性の重要性に焦点を当てた研究が増加しており20-22、MTase複合体の阻害は、新たながん治療法のアプローチになると期待されています。
m7G tRNA修飾:今後の治療法としての展望
上述したように、m7G修飾はtRNAのサブセットで発生し、修飾したtRNAの安定化、また正常なmRNAの翻訳に必要なものです。METTL1/WDR4 MTase複合体の欠損は、マウス幹細胞の自己複製と神経細胞の分化を阻害し、特定のヒトの発達障害の遺伝的要因となります。逆に、m7G MTase複合体の過剰な活性化は、腫瘍形成を促進します。いずれの場合も、機能的なtRNAプールと、それに続くmRNA の「トランスラトーム (translatome)」のリモデリングが表現型に関与しています。
mRNAの個々のサブセットには特定のコドンが偏って含まれており、それぞれに対応した異なるtRNAを必要とします。この「コドンバイアスを受けた翻訳」は、元々は酵母のストレス応答制御として特定されたものですが、この現象から、現在の遺伝コードの解釈は簡略化され過ぎていることがわかります。このことより、特定のtRNA修飾は、遺伝子の特定のサブセットにおけるmRNAの翻訳とタンパク質発現に対して、異なる効果を与える役割をもつと考えられます23。
tRNAエピトランスクリプトームとtRNAの欠損がヒトの疾患で果たす役割をより深く理解することにより、転写後の遺伝子調節を標的とする新たな治療法を開発することができます。例えば、METTL1は多くの異なるがんの発がんに関与しており、METTL1遺伝子のノックダウンまたはノックアウトは、様々なモデルマウスにおける腫瘍の成長を抑制することから、低分子薬を用いたこの酵素の阻害は新しいがん治療戦略となる可能性があります。急性骨髄性白血病 (AML) モデルマウスにおいて、N6-メチルアデノシン (m6A) MTaseであるMETTL3の化学的阻害剤が顕著な抗がん作用を示したことは、エピトランスクリプトームを操作したがん治療法の有望性をさらに裏付けるものです24, 25。また、METTL1はがん細胞の成長を促進するだけでなく、肝内胆管がん (ICC) モデルマウスにおけるがん微小環境や免疫チェックポイント阻害剤 (抗PD-1抗体) への治療応答性にも影響を与えます26。効果的な新たながん治療法の開発のために、METTL1の特異的な化学的阻害剤の特定が必要とされています。
m7Gは、150を超える既知のRNA修飾の1つであり、エピトランスクリプトームのより広範な探索への関心が急速に高まっています。これらの研究を前進させるには、個々の修飾の正確なマッピングを可能にする新たな方法と試薬が不可欠です。
追加リソース:
-
RNA修飾を含むRNA調節機構について探索してください
-
真核生物において最も豊富なmRNA修飾であるm6Aに関する詳細は、 カリフォルニア大学アーバイン校で微生物学および分子遺伝学の助教を務めるGina Lee博士にご寄稿いただいたm6A:細胞に秘められた遺伝子調節シグナルをご覧ください
参考文献:
-
Boccaletto P, Stefaniak F, Ray A, et al. MODOMICS: a database of RNA modification pathways. 2021 update. Nucleic Acids Res. 2022;50(D1):D231-D235. doi:10.1093/nar/gkab1083
-
Moshitch-Moshkovitz S, Dominissini D, Rechavi G. The epitranscriptome toolbox. Cell. 2022;185(5):764-776. doi:10.1016/j.cell.2022.02.007
-
Alexandrov A, Chernyakov I, Gu W, et al. Rapid tRNA decay can result from lack of nonessential modifications. Mol Cell. 2006;21(1):87-96. doi:10.1016/j.molcel.2005.10.036
-
Lin S, Liu Q, Lelyveld VS, Choe J, Szostak JW, Gregory RI. Mettl1/Wdr4-Mediated m7G tRNA Methylome Is Required for Normal mRNA Translation and Embryonic Stem Cell Self-Renewal and Differentiation. Mol Cell. 2018;71(2):244-255.e5. doi:10.1016/j.molcel.2018.06.001
-
Lin S, Liu Q, Jiang YZ, Gregory RI. Nucleotide resolution profiling of m7G tRNA modification by TRAC-Seq. Nat Protoc. 2019;14(11):3220-3242. doi:10.1038/s41596-019-0226-7
- Orellana EA, Liu Q, Yankova E, et al. METTL1-mediated m7G modification of Arg-TCT tRNA drives oncogenic transformation. Mol Cell. 2021;81(16):3323-3338.e14. doi:10.1016/j.molcel.2021.06.031
-
Marchand V, Ayadi L, Bourguignon-Igel V, Helm M, Motorin Y. AlkAniline-Seq: A Highly Sensitive and Specific Method for Simultaneous Mapping of 7-Methyl-guanosine (m7G) and 3-Methyl-cytosine (m3C) in RNAs by High-Throughput Sequencing. Methods Mol Biol. 2021;2298:77-95. doi:10.1007/978-1-0716-1374-0_5
-
Zhang LS, Liu C, Ma H, et al. Transcriptome-wide Mapping of Internal N7-Methylguanosine Methylome in Mammalian mRNA. Mol Cell. 2019;74(6):1304-1316.e8. doi:10.1016/j.molcel.2019.03.036
-
Pandolfini L, Barbieri I, Bannister AJ, et al. METTL1 Promotes let-7 MicroRNA Processing via m7G Methylation. Mol Cell. 2019;74(6):1278-1290.e9. doi:10.1016/j.molcel.2019.03.040
- Vinther J. No Evidence for N7-Methylation of Guanosine (m7G) in Human let-7e. Mol Cell. 2020;79(2):199-200. doi:10.1016/j.molcel.2020.05.022
- Alexandrov A, Martzen MR, Phizicky EM. Two proteins that form a complex are required for 7-methylguanosine modification of yeast tRNA. RNA. 2002;8(10):1253-1266. doi:10.1017/s1355838202024019
- Ruiz-Arroyo VM, Raj R, Babu K, Onolbaatar O, Roberts PH, Nam Y. Structures and mechanisms of tRNA methylation by METTL1-WDR4 [published online ahead of print, 2023 Jan 4]. Nature. 2023;10.1038/s41586-022-05565-5. doi:10.1038/s41586-022-05565-5
- Li J, Wang L, Hahn Q, et al. Structural basis of regulated m7G tRNA modification by METTL1-WDR4 [published online ahead of print, 2023 Jan 4]. Nature. 2023;10.1038/s41586-022-05566-4. doi:10.1038/s41586-022-05566-4
- Alexandrov A, Grayhack EJ, Phizicky EM. tRNA m7G methyltransferase Trm8p/Trm82p: evidence linking activity to a growth phenotype and implicating Trm82p in maintaining levels of active Trm8p. RNA. 2005;11(5):821-830. doi:10.1261/rna.2030705
- Filonava L, Torres AG, Ribas de Pouplana L. A novel cause for primordial dwarfism revealed: defective tRNA modification. Genome Biol. 2015;16:216. Published 2,015 Oct 1. doi:10.1186/s13059-015-0786-y
- Shaheen R, Abdel-Salam GM, Guy MP, et al. Mutation in WDR4 impairs tRNA m(7)G46 methylation and causes a distinct form of microcephalic primordial dwarfism. Genome Biol. 2015;16:210. Published 2015 Sep 28 doi:10.1186/s13059-015-0779-x
- Michaud J, Kudoh J, Berry A, et al. Isolation and characterization of a human chromosome 21q22.3 gene (WDR4) and its mouse homologue that code for a WD-repeat protein. Genomics. 2000;68(1):71-79. doi:10.1006/geno.2000.6258
- Pereira PL, Magnol L, Sahún I, et al. A new mouse model for the trisomy of the Abcg1-U2af1 region reveals the complexity of the combinatorial genetic code of down syndrome. Hum Mol Genet. 2009;18(24):4756-4769. doi:10.1093/hmg/ddp438
- Sahún I, Marechal D, Pereira PL, et al. Cognition and hippocampal plasticity in the mouse is altered by monosomy of a genomic region implicated in Down syndrome. Genetics. 2014;197(3):899-912. doi:10.1534/genetics.114.165241
- Dai Z, Liu H, Liao J, et al. N7-Methylguanosine tRNA modification enhances oncogenic mRNA translation and promotes intrahepatic cholangiocarcinoma progression. Mol Cell. 2021;81(16):3339-3355.e8. doi:10.1016/j.molcel.2021.07.003
- Ma J, Han H, Huang Y, et al. METTL1/WDR4-mediated m7G tRNA modifications and m7G codon usage promote mRNA translation and lung cancer progression. Mol Ther. 2021;29(12):3422-3435. doi:10.1016/j.ymthe.2021.08.005
- Han H, Yang C, Ma J, et al. N7-methylguanosine tRNA modification promotes esophageal squamous cell carcinoma tumorigenesis via the RPTOR/ULK1/autophagy axis. Nat Commun. 2022;13(1):1478. Published 2022 Mar 18 doi:10.1038/s41467-022-29125-7
- Dedon PC, Begley TJ. Dysfunctional tRNA reprogramming and codon-biased translation in cancer. Trends Mol Med. 2022;28(11):964-978. doi:10.1016/j.molmed.2022.09.007
-
Yankova E, Blackaby W, Albertella M, et al. Small-molecule inhibition of METTL3 as a strategy against myeloid leukaemia. Nature. 2021;593(7860):597-601. doi:10.1038/s41586-021-03536-w
-
Li J, Gregory RI. Mining for METTL3 inhibitors to suppress cancer. Nat Struct Mol Biol. 2021;28(6):460-462. doi:10.1038/s41594-021-00606-5
-
Liu H, Zeng X, Ren X, et al. Targeting tumour-intrinsic N7-methylguanosine tRNA modification inhibits MDSC recruitment and improves anti-PD-1 efficacy [published online ahead of print, 2022 Oct 25]. Gut. 2022;gutjnl-2022-327230. doi:10.1136/gutjnl-2022-327230
開示情報:Richard I. Gregoryは、Redona Therapeuticsの共同設立者、科学諮問委員、および株主であり、Cell Signaling Technologyのキーオピニオンリーダーキャンペーンに参加することで報酬を受け取っています。Gregory研究室は、Sanofi社、Astellas社、およびOno社より研究資金の提供を受けます(またはすでに受けています)。