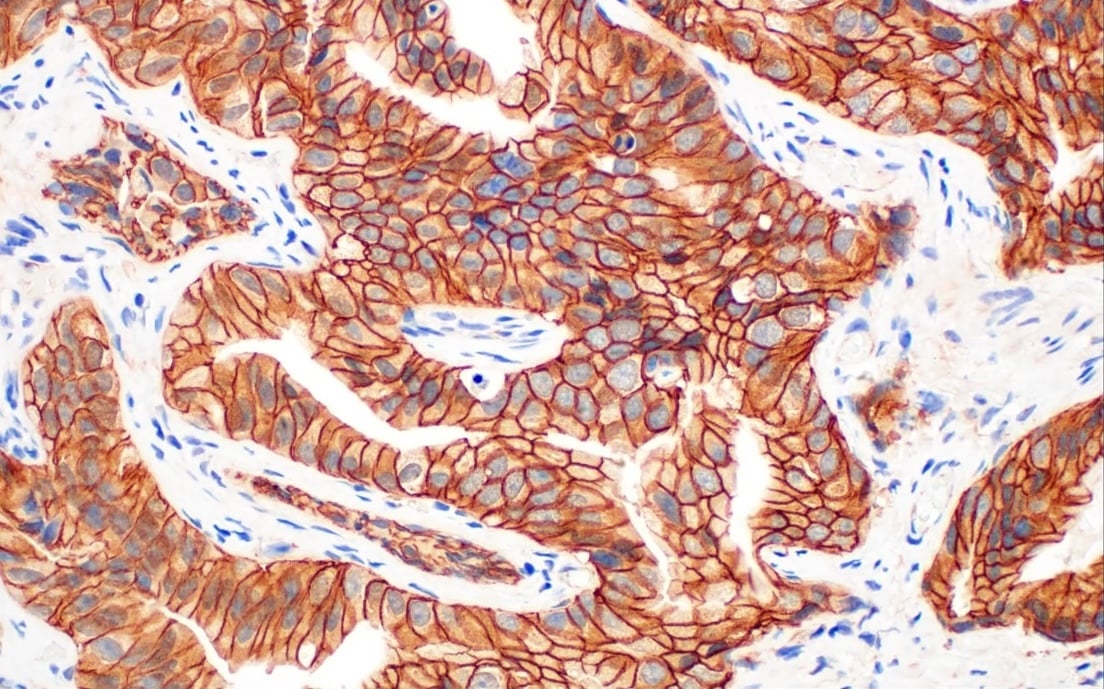
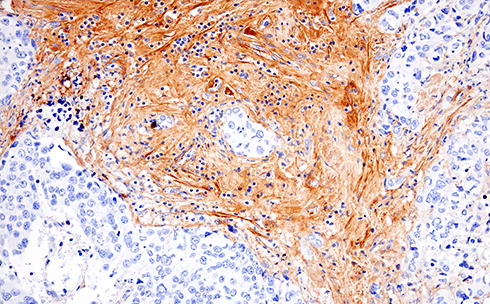
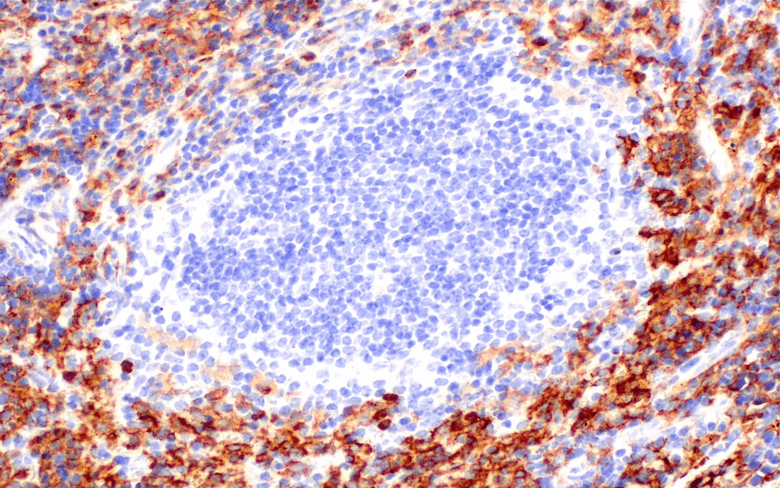
PrentzellらがCell誌に発表した論文では、約30種類のCST抗体を用いてG3BP1 (Ras GTPase-activating protein-binding proteins G3BP1) およびG3BP2の解析が行われています。これらのタンパク質は、ストレス顆粒 (SG) のマーカーとして広く利用されています。ストレス顆粒は、厳しい条件に晒された細胞の細胞質に形成されるmRNAとタンパク質の複合体であり、タンパク質の合成を抑制して細胞の生存を促進する機能を持っています。
 |
CSTが提供する関連抗体およびSamplerキットをご覧ください: • G3BP1 (E9G1M) XP® Rabbit mAb #61559 |
|
このPrentzellらの研究により、G3BPがTSC (Tuberous sclerosis complex) 複合体をリソソームにつなぎ止め、mTORC1 (Mechanistic target of rapamycin complex 1) のシグナル伝達を抑制することが分かってきました。mTORC1の過剰な活性化は、細胞の過剰増殖、遊走、神経細胞の興奮などを特徴とする疾患に関与するため、この発見は非常に重要です。これにより、G3BPはがんや神経疾患の重要な治療標的となる可能性が出てきました。
CST抗体は、全てHallmarks of Antibody Validation™に基づいて厳格に検証されているため、研究者は明確な結果を効率的に得ることができます。G3BPとTSC複合体との物理的な相互作用の確認や、mTORC1シグナル伝達の解明にも、この成果がみられた形になります。
< ブログの最後に記載する製品リストを見る場合はこちらをクリック >
G3BP1はストレス顆粒とは無関係に細胞内でmTORC1を阻害する
SGはmTORC1を阻害することが知られていますが、このプロセスへのG3BP1の関与はこれまで明らかにされていませんでした。そこでまず、著者らはMCF-7細胞を亜ヒ酸塩で処理してSGを誘導した場合と、SGを形成しない条件で培養した場合で、mTORC1活性を比較しました。
この結果、予想通り、亜ヒ酸塩処理によってmTORC1のリン酸化基質であるRPS6KB1 (Ribosomal protein S6 kinase B1) のT389のリン酸化 (RPS6KB1-pT389) が増強されました。しかし、G3BP1をノックダウンした細胞では、亜ヒ酸塩処理によるRPS6KB1-pT389レベルに影響がみられず、G3BP1はSGを形成した細胞のmTORC1活性に影響しないことが明らかになりました。
この他のデータとも組み合わせ、G3BP1によるmTORC1の阻害はSGとは無関係に起こり、G3BP1はSGの中心的な構成成分であることとは別に、他の機能を持つことが示唆されました。
G3BPはリソソーム表面に存在する
一連の研究により、G3BP1ノックアウト細胞でG3BP2はRPS6KB1-T389の高リン酸化を抑制しないことが分かり、SGの形成においてはG3BP1をG3BP2で代用することができるものの、G3BP1の欠損をG3BP2で完全に代償できるわけではないことが明らかになりました。この結果はG3BPがヘテロ複合体を形成することを示唆しており、G3BPがmTORC1を阻害する細胞内区画を特定する研究が進められました。
G3BP1とG3BP2は、TSC1、TSC2、TBC1D7からなるTSC複合体と同じ分画、すなわちリソソーム分画に存在することが示されました。これらの分画を調べると、G3BPはLAMP1 (Lysosomal associated membrane protein 1) タンパク質に近接して局在していることが明らかになりました。しかし、リソソームサンプルをトリプシンプロテアーゼで処理すると、主に内腔側のタンパク質であるLAMP1は分解されず、G3BPとTSC複合体は分解されてしまい、G3BPはTSC複合体とともにリソソーム表面に存在していることが示唆されました。
さらに、共免疫沈降法 (co-IP) やPLA (Proximity ligation assay) による解析で、G3BPとTSC複合体の物理的な相互作用が明らかになりました。特に、G3BP1をノックアウトした細胞は、TSC2を欠損した細胞と同様の表現型を示し、飢餓状態に陥ると肥大化してmTORのリソソームへの局在化が促進されているという知見は重要です。
G3BP1はTSC複合体を介してmTORC1を抑制する
G3BP1とTSC複合体が相互作用することから、TSC2の存在下と非存在下で、G3BP1の阻害がmTORC1活性に及ぼす影響が調べられました。コントロール細胞ではG3BP1の阻害によりRPS6KB1-pT389の誘導がみられるのに対し、TSC複合体を欠損するTSC2ノックアウト細胞では同様の結果がみられませんでした。これらの結果から、G3BP1とTSC複合体が同じ経路でmTORC1を抑制し、G3BP1がTSC複合体をリソソームにつなぎ止めていることが示唆されました。
 |
mTORシグナル伝達のインタラクティブパスウェイ図と、関連するCST製品をご覧ください。 |
治療的介入におけるG3BP1の標的化
G3BP1は、mTORC1の過剰なた活性化を特徴とする疾患の治療への応用の可能性を秘めています。今回の論文で、乳がん患者の無再発生存期間 (RFS) は、G3BP1のmRNAまたはタンパク質レベルが中央値以下の場合に短くなることが指摘されており、TSC1またはTSC2が低い患者のRFSが短いことと一致しています。このため、G3BP1を利用することで転移や腫瘍の成長の抑制し、患者の生存率を高められる可能性があります。
さらに今回の論文では、ゼブラフィッシュのG3BP1を阻害がmTORC1の活性を亢進することが、Ribosomal protein s6のSer235/236のリン酸化 (Rps6-pS235/236) の解析により実証されました。このような阻害がin vivoで生じると、mTORC1に依存して脳機能に影響を与えるTSC2欠損と同様の表現型が現れるため、G3BP1が神経系の発生と活動において極めて重要であることが分かります。これは、G3BPが神経疾患の治療において有用である可能性を示唆しています。
CST抗体製品一覧
紹介した研究論文で使用された抗体については、以下の製品リストをご覧ください。
G3BPの研究にどのようにCST抗体を用いたのか、また、どのようにしてこのタンパク質ががんや神経疾患の治療の標的になり得ることを明らかにしたのかについては、論文のフルテキストをご覧ください。