本ブログ記事では、ポリクローナル抗体とモノクローナル抗体の長所と短所をいくつか掘り下げ、また研究で用いるマウス抗体とラビット抗体の主な違いを説明します。抗体技術がどのように進化したかに関すしてまとめた抗体の必須知識Part 3で述べたように、信頼性の高い免疫アッセイの結果を得るためには正しい考え方を身に着けることが重要であるため、抗体をご自身で作製することを想定してご覧ください。
目次
抗体のクローン性とは?
以前、抗体の分類に関する抗体の必須知識Part 2で、分類の方法の1つとしてポリクローナル抗体とモノクローナル抗体に分ける方法を紹介しました。しかし、ご存知のように「クローニング」という用語は非常に柔軟で、遺伝子配列のコピーや編集、その遺伝子をもつ細胞の取り扱いや増殖を指すほか、さらには生物一個体すべてをクローニングするという意味で使われることもあります。
抗体におけるクローニングの意味を理解するためにまず、以前投稿した抗体の多様性の記事で紹介したように、活性化したB細胞が増殖することで免疫応答と抗体の産生が増強されることを思い出してください。例えば、10種類のエピトープをもつウイルスタンパク質で動物を免疫し、10種類のB細胞が活性化されたとします。これらのB細胞はそれぞれ細胞表面に、V(D)J組換えを経て生み出されたユニークな抗体を発現します。したがって、この外来タンパク質に応答したB細胞の増殖によって10種類の別々のB細胞集団が生み出され、それぞれの集団内のB細胞どうしはクローン的に関連します。1つのクローン集団内のすべての細胞は同じ祖先のB細胞の子孫であり、同じ抗体を発現するという点で機能的に同一となります。この場合、この宿主動物の血漿には同時に10種類のB細胞集団 (クローン) が存在して増殖し、抗体を産生します。この宿主から血液を採集して血清から抗体を精製すると、10種類の異なるB細胞クローンに産生された10種類の異なる抗体の混合物が得られます。したがって、これをポリクローナル抗体と呼びます。
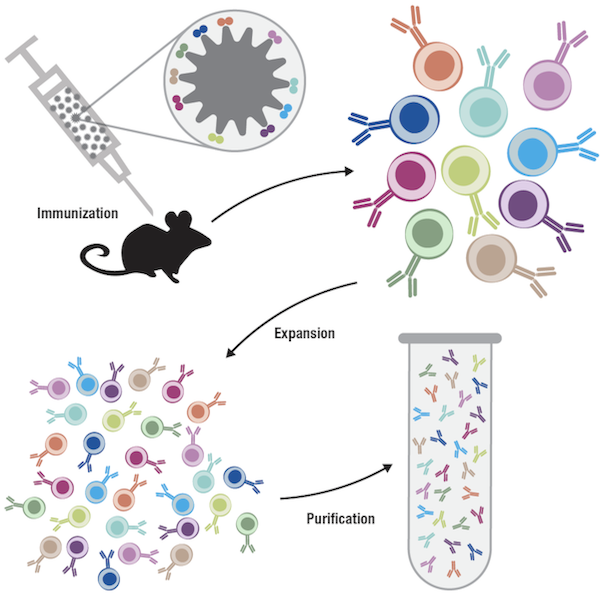
図1:ポリクローナル抗体は異なるB細胞クローンに由来する異なる抗体の混合物です
次に、血清を採集するのではなく、この免疫動物から全免疫細胞を単離してマルチウェルプレートで培養することを考えてみてください。1ウェル当たり0 - 1個の細胞が入るように細胞懸濁液を希釈して捲き込むと、もちろん後で試験を行い確認する必要はありますが、各ウェルでそれぞれに同一クローンの細胞を増殖させることができます。つまり、10種類のB細胞クローンのうちの1つが播かれたウェルで、同じ抗体を産生するクローン的に関連した純粋なB細胞集団を生育させることができます。しかし、B細胞は無限には増殖しないので、得られる抗体の量には限りがあります。
この欠点を克服するため、前回投稿した抗体の歴史に関するブログで紹介したように、1975年にKohler博士とMilstein博士によってハイブリドーマ技術が開発されました。脾臓細胞 (B細胞を含む脾臓の細胞集団) を不死化したミエローマ腫瘍細胞と融合させることで、不死化したハイブリドーマ細胞が形成されます。それぞれのハイブリドーマ細胞は祖先となったB細胞と同じ抗体を発現します。融合を起こした細胞のみが増殖する特殊な培地を用いて選択を行った後、モノクローナル細胞株を樹立するために限界希釈します。続いて細胞を増殖させ、試験と特性評価を行い、ハイブリドーマ細胞株を長期保存することで、長期的なモノクローナル抗体の供給源を確保します。1970年代以降に、細胞の不死化に依らずモノクローナル抗体を産生するリコンビナント法も開発されました。
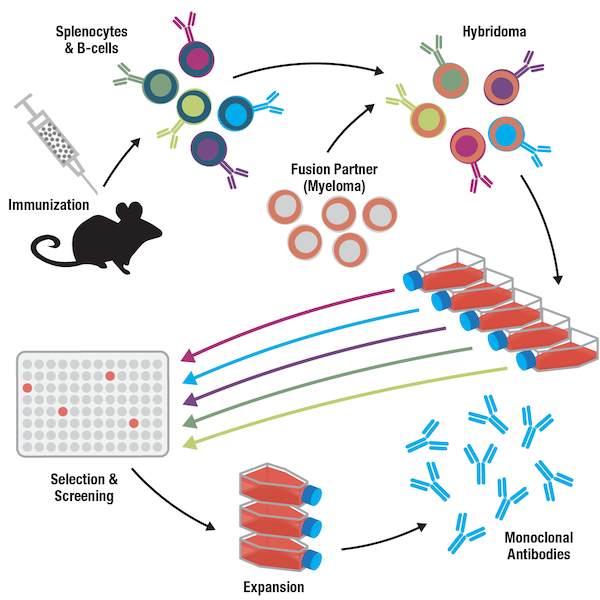 図2:モノクローナル抗体の産生には単離、選択、単一ハイブリドーマクローンの拡大のステップが必要で、これによって単一の抗体のみを調製することができます
図2:モノクローナル抗体の産生には単離、選択、単一ハイブリドーマクローンの拡大のステップが必要で、これによって単一の抗体のみを調製することができます
近年、ポリクローナル抗体とモノクローナル抗体の使用がともに大きく増加しています。どちらのタイプの抗体にもそれぞれ長所と短所があり、抗体の開発者やエンドユーザーによってどこに重点を置くかが異なるようです。過去数十年の間、学術研究者は多くの場合、自分たちで抗体の開発と検証を行い、研究に使用していたことを思い出してください。しかし、今日では開発者とユーザーの役割が別れていることが多くなっています。次に、研究用ポリクローナル抗体とモノクローナル抗体の長所と短所を、両方の役割の観点から探っていきます。
ポリクローナル抗体の長所と短所
まず、ポリクローナル抗体の長所を探ります。これは開発者とユーザーの両視点で一致する部分が大きいです。ポリクローナル抗体は短期間で安価に製造できるため、市場に出るのも早く、科学者はいち早くこれを入手して実験に利用し始めることができます。これは特に、生物学的に重要な役割をもつと推測されている新規タンパク質あるいはこれまで十分に研究されていなかったタンパク質など、関心が集まっている「ホットな」標的の場合は重要です。一般的に、「ホットな」標的に対するポリクローナル抗体はモノクローナル抗体より早く入手できるようになります。ポリクローナル抗体はラビットを宿主として製造されることが多いですが、ヤギやヒツジ、ロバなどを利用してより大量に生産することもでき、製造元にはより多くの材料、研究者には大規模スクリーニングをサポートするのに十分な抗体量を提供することができます。
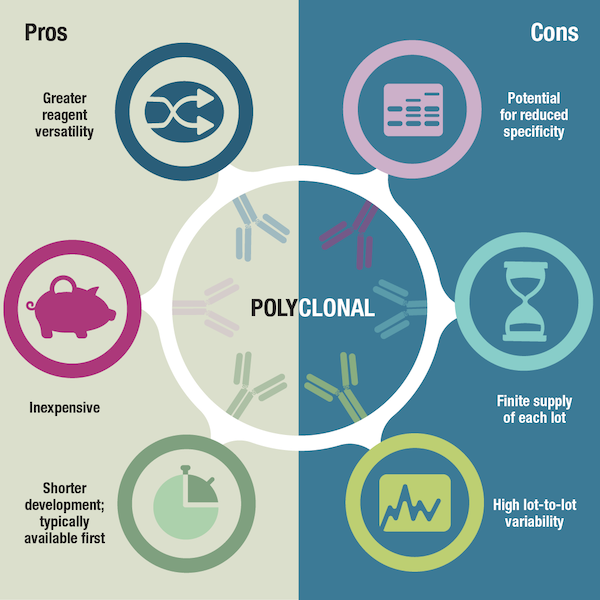 図3ポリクローナル抗体の長所と短所
図3ポリクローナル抗体の長所と短所
これらの長所に対してポリクローナル抗体の大きな短所として供給が宿主動物の寿命に制限される点が挙げられます。また、ポリクローナル抗体はロット間のばらつきが大きくなります。これは同じ動物から時間をかけて採集されたり、別の動物から採集されたりするためで、どちらの場合もポリクローナル抗体のロット間で組成が変化する原因となります。このため、抗体の提供元は新しく製造したロットの検証を継続的に行い、適切な代替製品を開発することが求められます。同じ理由で、研究者は抗体のロットが変わる場合には実験条件を再度最適化したり、アッセイの流れを再構成したりする必要があることもあります。また、ポリクローナル抗体はモノクローナル抗体に比べて特異性が低くなりがちであることも短所と言えます。ポリクローナル抗体はエピトープが異なる複数の抗体で構成されるため、非特異的な反応性をもつ可能性が高くなります。
モノクローナル抗体の長所と短所
次に、モノクローナル抗体に移ります。モノクローナル抗体の主な長所は、単一のエプトープのみを認識するため、特異性が高くなることです。モノクローナル抗体は開発段階で最良のクローンのスクリーニングと選択を行うので、この段階で最適化が成されます。抗体の開発者にとっては、特異性の高いモノクローナル抗体を作成することで、市場における他の製品に対する競争力を得ることができます。一方、研究者にとっては、ポリクローナル抗体に比べて免疫アッセイにおける標的の同定が容易になり、バックグラウンドが低下するという利点があります。論文を一報作成するため、または一連の論文を作成するために数ヶ月、1年、あるいは数年にわたって実験やコントロールを行う研究室もあります。異なる実験、異なる研究は互いに比較できることが望ましく、また新たな発見は他の研究室でも再現してそれを補強することが望ましいので、試薬の特異性や性能が大きく変わらないことが重要です。
概して、モノクローナル抗体は性能が安定しており、長期生産が保証され、比較的簡単にスケールアップできると言われています。このため、提供元は安定供給ができ、研究者は研究計画のスケジュールに依らず信頼性の高い実験ができるという利点があります。このような多くの長所に対し、モノクローナル抗体の短所はポリクローナル抗体に比べて開発に時間と費用がかかるということです。モノクローナル抗体がまだ開発されていない場合はひとまず既存のポリクローナル抗体を使用し、モノクローナル抗体が開発されたらそちらに切り替えるのも1つの方法です。
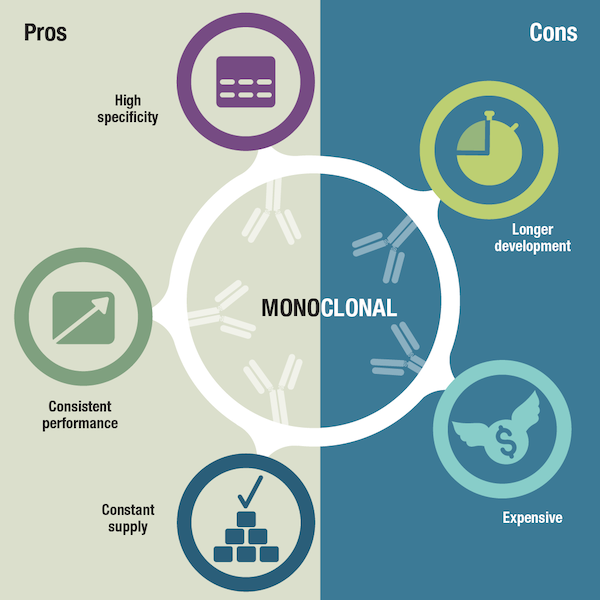 図4:モノクローナル抗体の長所と短所
図4:モノクローナル抗体の長所と短所
最終的にモノクローナル抗体とポリクローナル抗体のどちらを使用するかについては、実施を予定しているアッセイにおける必要性、実験目的を満たす抗体の費用と入手が可能であるかどうかなどを考慮して判断する必要があります。
長所と短所:宿主種としてのラビットとマウス
研究用一次抗体試薬として最もよく利用されているのはラビット抗体とマウス抗体です。以前はモノクローナル抗体開発における宿主動物種はマウスであることが一般的でした。これは、ハイブリドーマを作成するためにラビットのB細胞と融合させるパートナーになる適切な細胞が無かったためです。しかし、1995年にKatherine Knight博士の研究グループが形質細胞腫の細胞株を作成するためのトランスジェニックラビットを開発し、状況が変わりました。この結果、今日ではラビットのモノクローナル抗体も広く利用されています。抗体の産生にラビットを利用する利点は、ラビットはマウスに比べて免疫レパートリーがより多様であることです。このため、低分子ペプチドや生体低分子など、より広範囲の抗原に対して免疫応答を起こすことができます。また、ラビット抗体は通常、標的に対してより高いアフィニティーをもちます。抗体開発者の視点からは、多様性とアフィニティーが向上することでより広範な高選択性抗体が製造できることを意味し、研究者の視点からは、より多くの抗体試薬の中から選択できるようになることを意味しています。
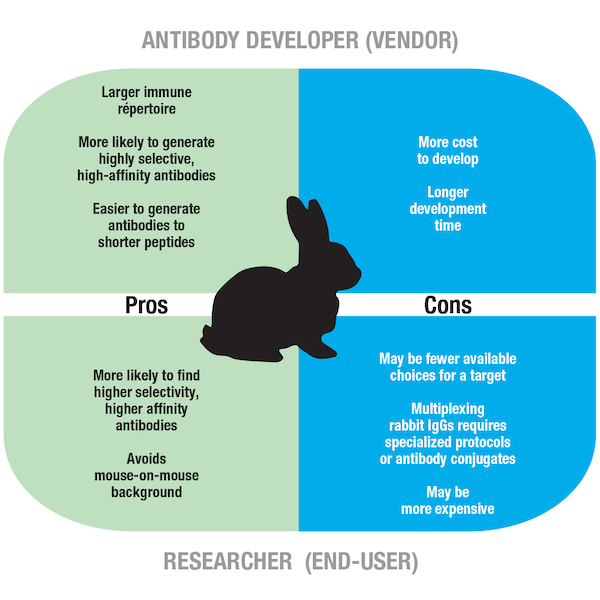 図5:モノクローナル抗体開発にラビットを宿主種として使用することの長所と短所
図5:モノクローナル抗体開発にラビットを宿主種として使用することの長所と短所
多様性とアフィニティーに優れるものの、ラビットモノクローナル抗体の製造には、やはり製造元にとっては非常に多くの時間と費用がかかるという短所があり、このため消費者にとってもマウスモノクローナル抗体より高価になりがちです。
同じアッセイで複数のラビットIgGを組み合わせて用いることを計画している方は、マルチプレックスIHCのための標識とストリッピング戦略などの、より複雑で困難なマルチプレックス (多重解析) プロトコールを検討する必要があります。また、マルチプレックスアッセイにおいて異なる蛍光色素で標識した抗体を利用することで、二次抗体を使用することなく直接検出を行うことができますが、必要な組み合わせの抗体と蛍光色素が入手できるかどうかが制約要因になることもあります。
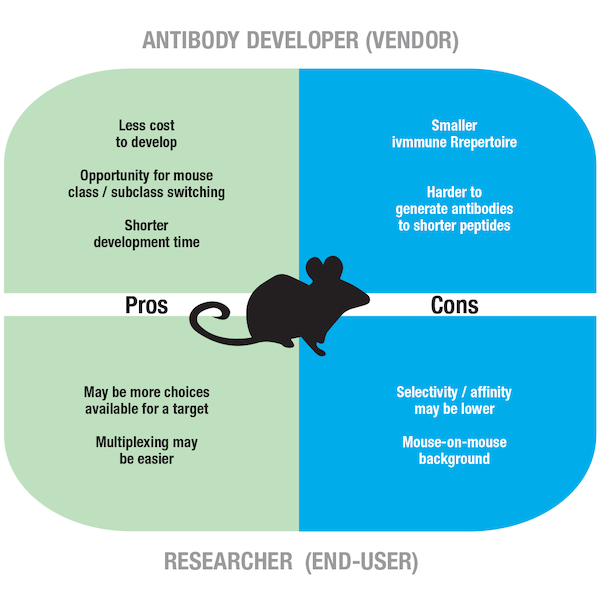 図6:モノクローナル抗体開発にマウスを宿主種として使用することの長所と短所
図6:モノクローナル抗体開発にマウスを宿主種として使用することの長所と短所
マウスモノクローナル抗体技術はラビットより長い間利用されてきたため、標的に対する抗体がラビット宿主のクローンのものよりマウス宿主のクローンのもの方が多い場合があります。また、開発者にとっての長所に、ラビット抗体には1つのクラスしか無いのに対してマウス抗体ではサブクラスの切り替え (例:IgG1、IgG2a) が可能な点が挙げられます。抗体ユーザーにとっても、クラスやサブクラスの異なるマウス抗体を用いることでマルチプレックス解析が比較的容易になります。抗体開発者の立場からは、マウスの方がラビットより飼育が容易です。さらに、リコンビナント技術における抗体の遺伝子工学的アプローチはラビットよりマウスの方が進んでおり、抗体の製造にはマウスの方が優先的に利用されることも多いです。
抗体の製造元にとって、マウスはラビットより多様性が低いこと、マウスでは低分子ペプチドや生体低分子に必ずしも適切な免疫応答が起こらないことが短所になります。研究者にとっては、マウス検体を解析する場合に、抗マウス二次抗体がマウスの内因性免疫グロブリンに交差して意図しないバックグラウンドを生じる「Mouse on mouse」の問題があります。これはマウス疾患モデルが日常的に利用されているIHC実験でよく起こる問題で、免疫染色にMouse on mouseブロッキングステップを組み込んだ拡張プロトコールを使用することで解決することができます。
詳細はこちら: mIHCとmIF用のさまざまなマルチプレックス技法の利点と欠点
今回はポリクローナル抗体とモノクローナル抗体、ラビット抗体とマウス抗体の長所と短所を説明しました。これら重要な試薬を皆様の研究計画にどのように適合させるか、目的の抗体を入手できないことがあるのは何故か、という疑問の解決に役立てば幸いです。マウス、ラビット、あるいはその他の生物種で産生したの抗体を使用するいずれの場合でも、信頼性の高いデータを得るにはアプリケーションや解析対象のタイプに応じて検証を行う必要があります。次回は研究に使用する抗体を選択する場合にどのようなことを考慮すべきかを説明します。
抗体の必須知識シリーズをご覧ください:
- 抗体の必須知識 Part 1:抗体の基礎
- 抗体の必須知識Part 2:抗体の多様性と分類
- 抗体の必須知識Part 3:抗体技術の進歩
- 抗体の必須知識Part 4:ポリクローナル抗体とモノクローナル抗体
- 抗体の必須知識Part 5:抗体の選択における重要な検討事項
20-FLE-62535