社会の高齢化が進むにつれて、神経変性や認知症の症例が増加すると予測されていますが、アルツハイマー病 (AD) やパーキンソン病 (PD) などの疾患には治療法がありません。効果的な治療戦略を開発するためには、これらの神経変性疾患の病因に関連する様々な細胞タイプについてや、異なる細胞タイプがどのように相互作用しているかなどを、より深く理解する必要があります。すべての事象にあてはまることですが、物事の本質を理解することが重要です!
これらに関する知見を得る方法の1つに、マルチプレックス空間プロファイリング技術があります。この手法は、がん微小環境 (TME) 内のタンパク質や転写産物のマッピングを可能にする、腫瘍学の研究における非常に重要な技術であり、細胞の動態が臨床転帰にどのように影響するかを明らかにするのに役立ちます。脳におけるマルチプレックス空間プロファイリング技術は、アミロイドβ (Aβ) 斑や神経原線維変化 (NFT) といったADの病理学的特徴を示す細胞の特性解析を可能にするなど、神経変性研究においても同様に役立つ可能性を秘めていますが、まだ十分に活用されていません。
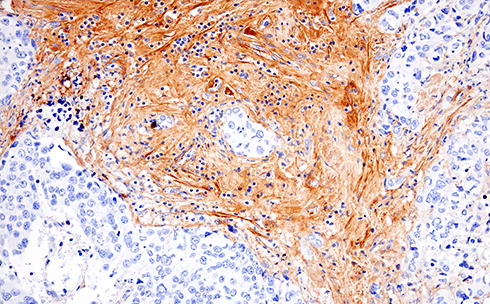
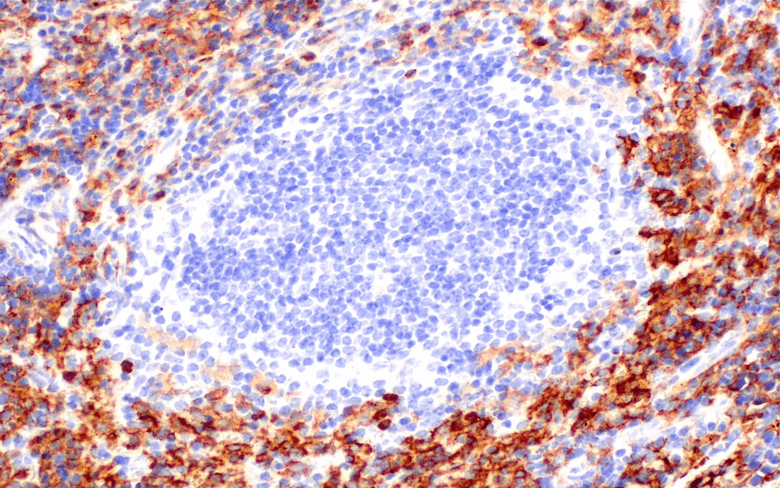
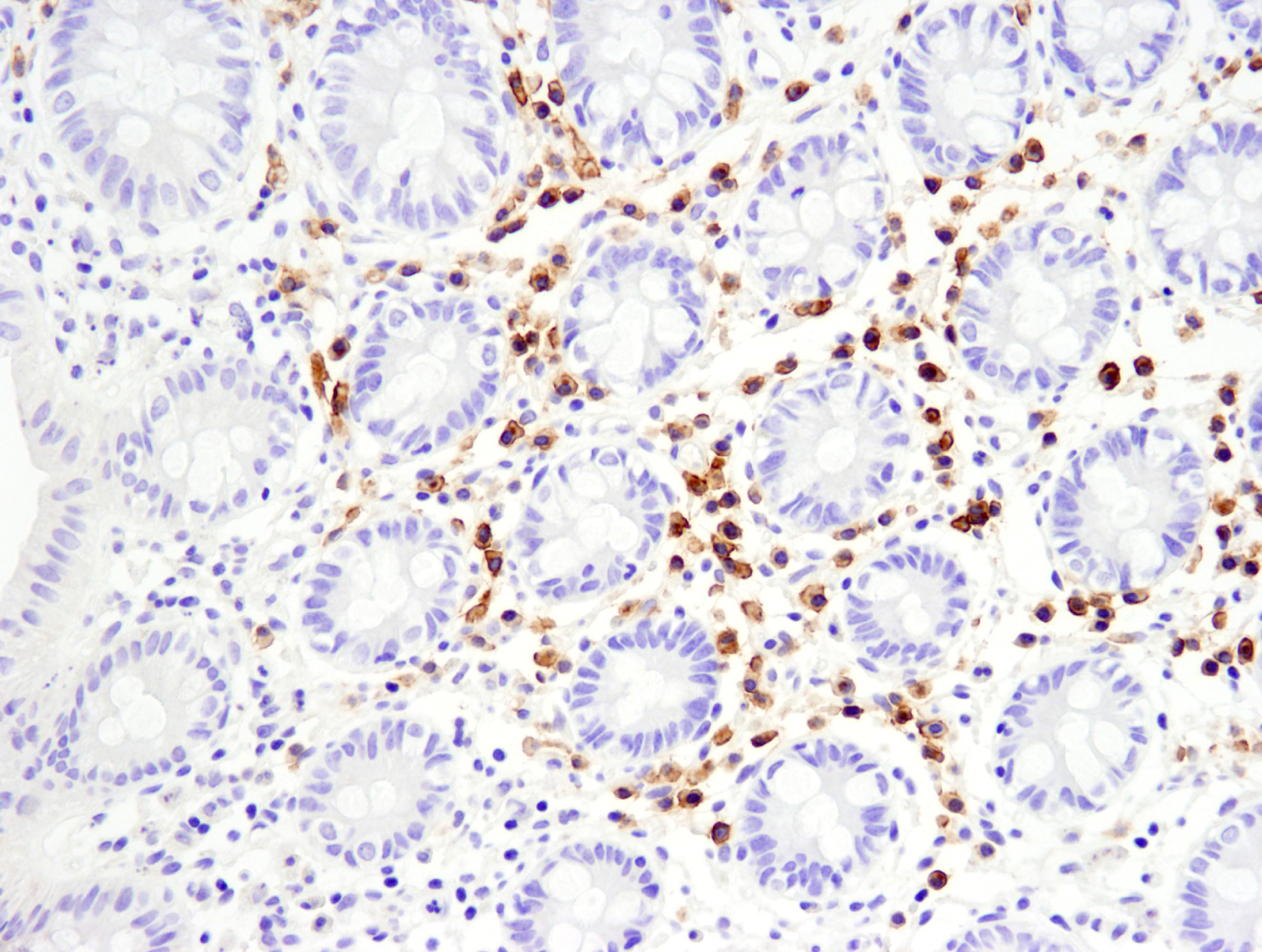
 空間プロファイリングのマルチプレックス解析により、成人のアルツハイマー病ヒト脳組織では、リン酸化Tauを含む神経原線維変化やAβ斑が有意に増加していることが分かります。画像は、「Spatial Proteomic Analysis of Alzheimer’s Disease Human Brain using Multiplexed Imaging.」のポスターから引用しています。
空間プロファイリングのマルチプレックス解析により、成人のアルツハイマー病ヒト脳組織では、リン酸化Tauを含む神経原線維変化やAβ斑が有意に増加していることが分かります。画像は、「Spatial Proteomic Analysis of Alzheimer’s Disease Human Brain using Multiplexed Imaging.」のポスターから引用しています。
神経変性の研究者が直面する問題の1つは、サンプルの性質に起因します。神経変性研究用のサンプルは、特に入手が困難であり、マルチプレックス空間プロファイリングを行うには独特な課題がいくつか存在します。ヒト脳組織では、疾患状態を直接調べることができますが、マウスや細胞を用いたモデルとは異なり、その多くがホルマリン固定やパラフィン包埋 (FFPE) されます。一方、マウスサンプルは通常、凍結保存されます。そのため、両サンプルの染色に常に同じ抗体を用いることができず、比較が困難になります。また、これまでは、研究者がFFPE組織を用いた発色による解析を行うには、多大な時間と労力の両方が必要となるシングルプレックスを複数回行う方法しか選択肢はありませんでした。また、Lipofuscinの蓄積による自家蛍光や、確実に正確な染色を行うのに十分な特異性と感度を持つ検証済み抗体の不足は、さらなる問題を引き起こします。
本ブログ記事では、脳組織におけるタンパク質のマルチプレックス検出に利用可能な免疫組織化学染色 (IHC) 法、特にFFPE処理された組織の染色に着目して解説します。また、Leica Microsystems社のマルチプレックスイメージングソリューションCell DIVEと弊社のIF/IHC検証済み抗体と組み合わせることにより、ADの脳サンプルを空間的および分子的にどのように特性解析できるかについても紹介します。
ヒトの脳を理解するのに、なぜ空間プロファイリングが重要なのか?
フローサイトメトリーやsingle-cell RNA sequencing (scRNA-seq) などのシングルセル解析技術は、生物学的サンプルの特性解析に広く用いられていますが、本来の組織環境における様々な細胞タイプの局在を明らかにすることはできません。細胞間の相互作用が疾患の病因となることも多いため、これらの解析手法では、貴重な情報を見逃す可能性があります。
例えば、脳において、細胞の恒常性の維持や免疫応答、細胞デブリの除去、毒性障害による損傷の検出や修復、血液脳関門の維持などにミクログリアとアストロサイトは不可欠です。しかし、その役割は非常に複雑であり、これらの細胞タイプは、時にジキルとハイドのような性格と例えられるような二面性を示すことがあります。ミクログリアとアストロサイトは、通常は神経を正常に保つサポートを行いますが、疾患または損傷に応答した際に、慢性的な炎症や神経変性、回復の阻害などを引き起こす可能性があります。さらに、グリア細胞 (特にミクログリア) は、遺伝性の神経変性疾患と関連しており、これらの細胞が疾患の病因において直接的または間接的な役割を果たしている可能性があります。これらのグリア細胞が示す、空間的配置および一過性の様々な活性化パターンを解明し、異なる機能を持つ集団の特定に役立つ分子シグネチャーを同定することにより、ADやPDのような神経疾患の新たな治療法が発見できるかもしれません1 。
また、空間プロファイリング技術は、細胞の動態を調べるために不可欠です。この技術により、研究者は「各細胞タイプが何個存在するか?」といった基本的な質問から、「細胞は、どのようにして疾患状態に適応し、疾患の進行を直接遅らせたり早めたりするか?」や「Aβ斑やNFTのような病理学的特徴が、どのように細胞応答を促進するか?」といったより複雑な解析へと移行できます。
結局のところ、ますます複雑化する疑問に対する答えを得る方法が、効果的な治療戦略の開発に役立つのです。
空間プロテオミクスの利点とは?
空間プロテオミクスは、空間トランスクリプトミクスや空間ゲノミクスなどの他の形態の空間プロファイリングとは異なり、その最大の利点は、細胞機能についての知見が得られることです。なぜなら、タンパク質は、mRNAやDNAとは対照的に、細胞の挙動を直接制御する役割を担うからです。様々な疾患状態におけるmRNAシグネチャーが同定されていますが、それらは必ずしもタンパク質発現と相関するわけではありません。つまり、トランスクリプトームのデータを正しく解釈するためには、慎重な検証が必要です。
また、空間プロテオミクスは、神経変性疾患において調節不全となることが多い、翻訳後修飾 (PTM) の解析も可能にします。例えば、微小管関連タンパク質であるTauは、AD患者の脳では高度にリン酸化されていることが知られており、細胞毒性を有するTau凝集体であるNFTの形成につながります。一方、あまり知られていないTauのPTMであるO-GlcNAcylation (O-GlcNAc) は、Tauが高度にリン酸化されるのを抑制するため、AD患者に治療効果をもたらす可能性があると考えられています2。
脳組織サンプル研究用抗体
貴重な脳組織サンプルを用いて空間プロテオミクスデータを作成する際は、使用するアプリケーションで検証済みの抗体を選択することが最も重要です。FFPE組織でのIHC染色で検証されている抗体が、凍結組織サンプルでも機能すると考えている方も多いですが、機能しないこともよくあります。FFPE組織は、ホルムアルデヒド固定や脱パラフィン、抗原賦活化などの過酷な処理工程によりエピトープが損傷している可能性があるため、これらを使用する際は、FFPE組織サンプル用として厳密に検証された抗体を使用する必要があります。
CSTは、抗体の開発および試験を行う際は、厳格な検証基準に従い、アプリケーションやプロトコールごとに検証データを作成しています。なぜなら、弊社は、25年にわたる高品質な抗体の開発に取り組む過程において、あるアプリケーションで機能することが確認できても他のアプリケーションで機能することが保証されるわけではないことを早くから知っていたからです。弊社は、新鮮な凍結組織で検証された抗体の幅広い製品ラインナップに加えて、FFPE組織での使用が検証された800種類以上の抗体を提供しています。
以下の表に、ADバイオマーカーや他の神経疾患の研究用の主な抗体と、検証を行った組織タイプをまとめています:
また、FFPE組織または凍結組織用の、弊社のIHC検証済み抗体製品カタログもご覧ください。
空間プロテオミクスを用いた解析方法
FFPEに適した抗体を選択するのであれば、ますます増加する様々な空間プロテオミクス解析手法を使用できます。FFPE脳組織を使用する以下の手法では、複雑さや測定可能なマーカー数が異なります。また、CSTは、以下の手法をサポートしています:
- Leica Cell DIVE: Cell DIVE検証済みCST抗体を使用し、FFPE組織を最大4種類の蛍光標識抗体で順次染色します。サイクル間では、穏やかに化学標識を不活性化します。
- 直接検出法を使用した従来のIHC:蛍光標識一次抗体を用いて直接検出を行うため、間接検出よりもプロトコールのステップ数が少なく、二次抗体による交差反応のリスクを回避できます。
- 複数の生物種を用いたマルチプレックス検出: 異なる宿主種 (マウスやウサギ、ヤギなど) の一次抗体を、異なる蛍光色素で標識した各宿主種に特異的な二次抗体と組み合わせて使用することにより、1回の染色で3-5種類の標的を同時に検出できます。
- SignalStar® Multiplex IHC: SignalStar技術は、高い感度と特異性をもって、FFPE組織内の複数のバイオマーカーを同時に増幅します。オリゴヌクレオチド標識抗体を最大8種類の異なる標的に結合させた後、蛍光標識済みの相補的なオリゴヌクレオチドを用いて標的のシグナルを検出できるレベルまで増幅させます。
以下の研究ポスターでは、AD患者の脳組織のAβやTauの発現部位におけるアストロサイトやミクログリア、神経細胞などの細胞集団の空間的配置の同定や神経伝達の計算科学的な試験に、Leica Cell DIVEをどのように使用できるかを詳しく説明しています。詳細とポスターのダウンロードはこちら:
マルチプレックス手法の詳細については、以下のブログも参照してください:
神経変性研究における今後の課題
神経変性に対する研究者の理解が深まるにつれて、脳の空間的プロファイリングを可能にする手法も進化していく必要があります。様々な抗体が、すでにADやその他の神経変性疾患の細胞動態を解析するために幅広く使用されています。今後の課題としては、同時検出できるタンパク質の数を数十から数百まで拡大すること、新たに発見されたバイオマーカーに対応する抗体製品を製造すること、疾患との関連において細胞のマルチオミクス解析を行うためのれまで以上に洗練されたツールや技術を開発することなどが挙げられます。
参考文献
- Wu Y, Eisel ULM. Microglia-Astrocyte Communication in Alzheimer's Disease. J Alzheimers Dis. 2023;95(3):785-803. doi:10.3233/JAD-230199
- Zhu Y, Shan X, Yuzwa SA, Vocadlo DJ. The emerging link between O-GlcNAc and Alzheimer disease. J Biol Chem. 2014;289(50):34472-34481. doi:10.1074/jbc.R114.601351
24-NDT-91551