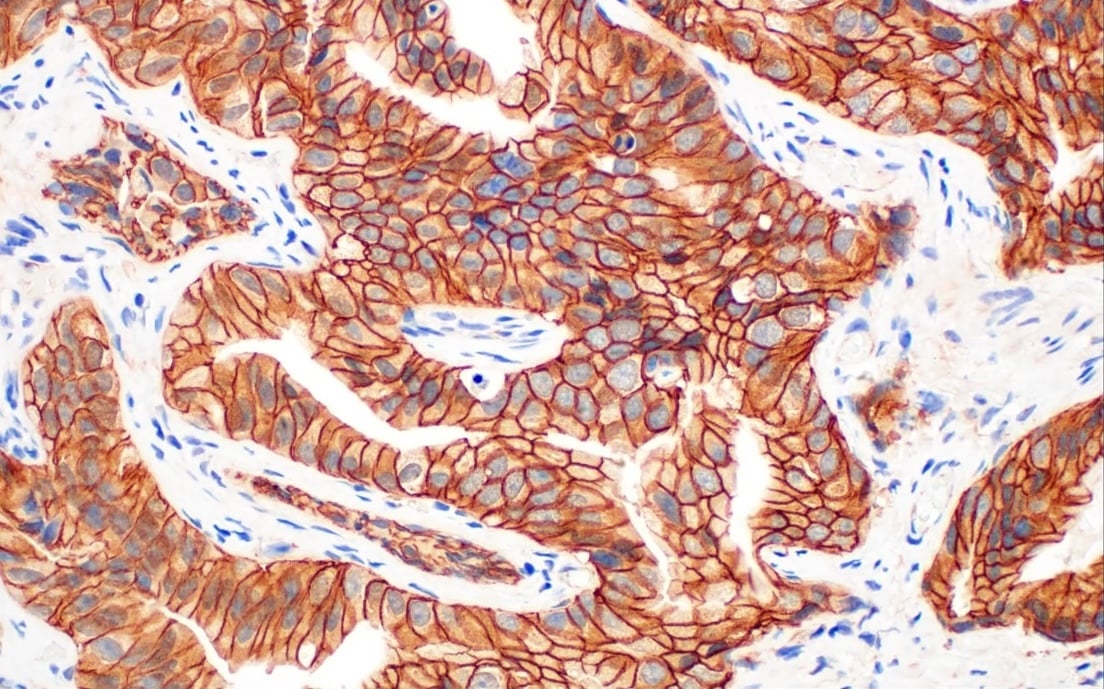
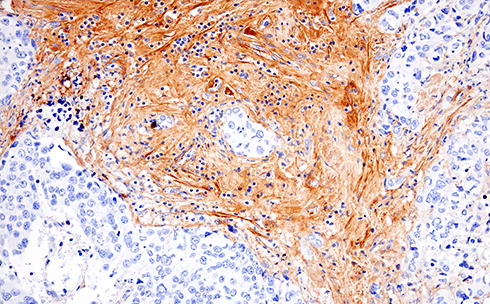
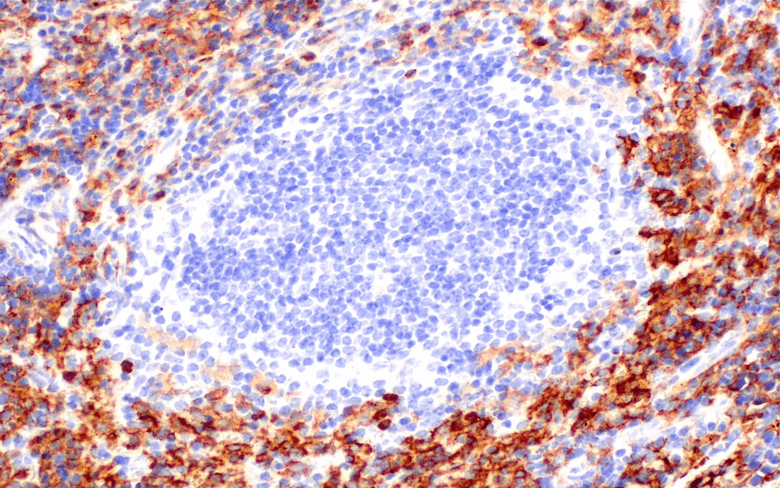
がん細胞は、腫瘍に栄養素を供給するために新しい血管の形成を誘導します。血管新生は、既存の血管から新たな血管枝を形成して血管網を構築する現象です。これは、腫瘍の増殖において重要な役割を果たします。

血液の供給が不十分である場合、良性腫瘍は休止状態のまま維持される可能性があります。しかし、休止状態の腫瘍で血管新生が活性化し、新たな血管の出芽や血管内皮細胞の腫瘍塊への走化性を誘導する増殖因子が分泌されると「血管新生スイッチ」が起こります。
低酸素状態の腫瘍塊では、HIF-1 (hypoxia inducible factor-1) が安定発現し、HIF-1は、VEGF (vascular endothelial growth factor) やbFGF (basic fibroblast growth factor)あるいはPDGF (platelet-derived growth factor) といった、いくつもの遺伝子の発現を活性化させて血管新生のプロセスに寄与します。
本ブログ記事で紹介した、がんの特性の1つである「血管新生」に関連するタンパク質についてもっと詳しく知りたい方は、以下の血管新生リソースのリンクをご覧ください。
- 血管新生リソース
がんの特性研究の標的に関する、完全なガイドをご覧ください。 eBookのダウンロードはこちら
Robert Weinberg博士とDouglas Hanahan博士によって特定されたがんの特性に関する論文は、まずはCell誌で発表されてました1。この著者らは、がんの複雑さを、より基本的な原理に基づく小さなサブセットに分解して捉えることを推奨しています。ここでは、これらの各サブセットのうちの1つを解説しています。このシリーズの他の記事では、他の既知の特性について解説しています。
詳細は「がんの特性」シリーズのブログをご覧ください。
- 細胞死への抵抗性
- 細胞エネルギー代謝の調節解除
- 増殖シグナルの持続
- 無秩序な複製による不死化
- 増殖抑制の回避
- 浸潤能および転移能の活性化
- 腫瘍による炎症の促進
- ゲノムの不安定性と変異
- 免疫による排除の回避
- Hanahan D, Weinberg RA (January 2000). "The Hallmarks of Cancer". Cell. 100 (1): 57–70. doi:10.1016/S0092-8674(00)81683-9
- Hanahan D, Weinberg RA (March 2011). "Hallmarks of Cancer: the next generation". Cell. 144 (5):646-74. doi: 10.1016/j.cell.2011.02.013.