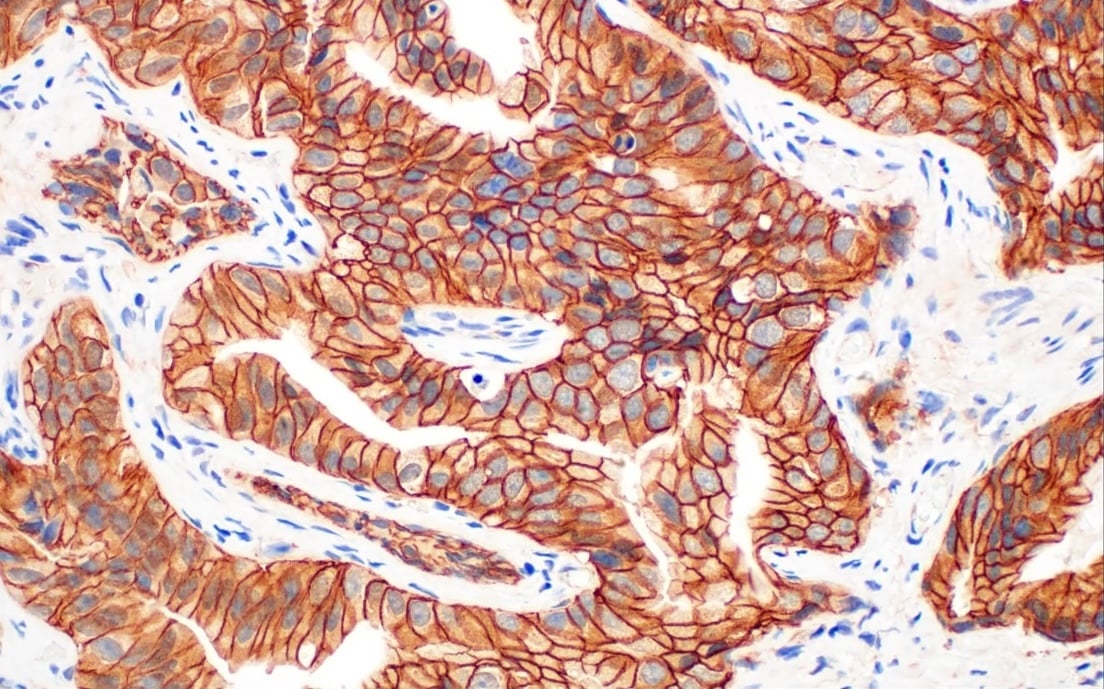
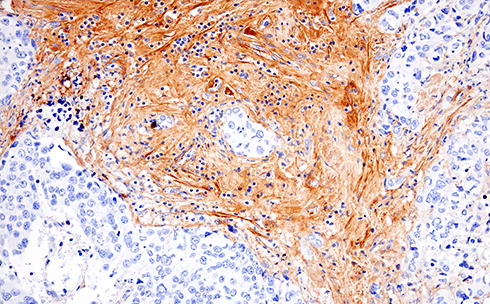
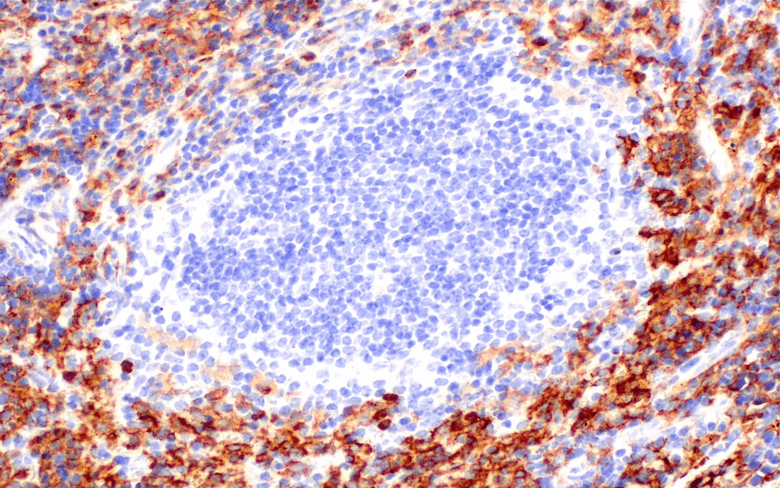
がん細胞は、炎症メカニズムを乗っ取り、自らの増殖と生存を促進します。自然免疫系および適応免疫系による正常な炎症応答の場合、免疫細胞は外来からの侵入者の貪食または破壊、あるいはその両方を行います。

がんの特性 (Hallmarks of cancer) はRobert Weinberg博士とDouglas Hanahan博士によって提唱され、Cell誌に発表されたものです。彼らは、複雑ながんの性質を、より小さな特性に細分化して捉えることを提案しています。今回の記事では「炎症を促進する腫瘍」と題し、がんの特性の1つに関連する内容を記載しました。本シリーズの他の記事では、今回触れなかった他の特性についても解説します。
感染と戦うこれらの免疫細胞は、複雑ながん微小環境下ではがん細胞により抑制されています。その結果、抗腫瘍免疫細胞は、形質転換した細胞を破壊することなく、腫瘍促進性の免疫細胞へと転換し、がん細胞の生存や遊走を促進する因子および免疫細胞による検出を阻止する因子を分泌することにより、腫瘍の増殖と転移を可能にします。がん微小環境における、免疫応答を仲介する重要な分子およびシグナル伝達経路には、NF-κBやインフラマソームシグナル伝達、腫瘍浸潤性免疫細胞マーカー、免疫チェックポイントシグナル伝達などがあります。
NF-κB
免疫細胞では、NF-κBシグナル伝達が遺伝子の転写を制御し、自然免疫および適応免疫、炎症、ストレス応答、B細胞の分化、サイトカイン/ケモカインの放出に影響を与えます。未刺激の細胞では、NF-κBは、細胞質にてIκBを阻害するタンパク質と複合体を形成しています。細胞が活性化されると、IκBタンパク質はリン酸化され、ユビキチン-プロテアソーム系により迅速に分解されます。IκBタンパク質が分解されると、それまで細胞質に留められていたNF-κBは、核内に移行し、遺伝子発現を制御します。
インタラクティブパスウェイ図:NF-κBシグナル伝達
がん微小環境内のがん細胞および免疫細胞におけるNF-κBシグナル伝達は、腫瘍との境界に存在する細胞の上皮間葉転換 (EMT) と特に関連しており、がん細胞の腫瘍塊の剥離および遊走を引き起こします。EMTは、悪性がんの特性として昔から知られています。そのため、免疫浸潤細胞とがん細胞におけるNF-κBシグナル伝達間のクロストークは、循環的なフィードフォワードにより、腫瘍の増殖や浸潤、悪性化を促進する環境を確立します。
インフラマソームシグナル伝達
自然免疫系は、病原性微生物および宿主に由来する細胞傷害のシグナルからの保護における、最初の防衛線になります。これらの「危険」シグナルが炎症を引き起こす経路の1つに、細胞質で形成されるタンパク質複合体であるインフラマソームの活性化があります。インフラマソームは、Caspase-1の切断と、その後の炎症性サイトカインIL-1βおよびIL-18の切断を促進します。
インタラクティブパスウェイ図:インフラマソームのシグナル伝達
特性解析が最も進んでいるインフラマソーム複合体はNLRP3複合体であり、この複合体には NLRP3、ASC (アダプタータンパク質) およびその他多数のタンパク質が含まれています。
腫瘍浸潤マーカー
免疫系は、自然免疫系および適応免疫系によりがん細胞を特定し排除しますが、このような抗腫瘍応答は、免疫抑制として知られるプロセスを介して、微小環境により阻害されます。がん免疫療法の目的は、免疫抑制および免疫刺激の両方のメカニズムを操作し、抗腫瘍免疫応答を高めることです。したがって、腫瘍の増殖と抑制における、腫瘍浸潤性免疫細胞の役割を理解することが重要です。
腫瘍浸潤性免疫細胞は、骨髄系細胞あるいはリンパ系細胞のいずれかに由来します。がん微小環境における免疫細胞の数とサブタイプは、予後と相関します。さらに、さらに、これら2つの起源のより詳細な解析は、各患者に適した免疫療法戦略の開発につながる可能性があります。
いったん腫瘍が形成されると、抗原の消失や主要組織適合分子の下方制御、内在性抗原提示経路の変化、サイトカイン分泌を介した免疫抑制など、様々なメカニズムを通じて免疫による検出が回避されます。腫瘍は、免疫系による検出を回避する能力に加えて、免疫細胞を乗っ取って自己増殖と転移を促進することもできます。腫瘍による免疫の抑制と破壊は通常、段階的に起こります。
免疫チェックポイント
免疫チェックポイントとは、自己寛容を維持し、生理学的な免疫応答による副次的な損傷の回避をサポートする、免疫系に組み込まれた制御メカニズムを指します。腫瘍は、免疫系による監視および攻撃を回避するため、特定の免疫チェックポイント経路を変化させることにより、微小環境を操作していることが分かっています3。
インタラクティブパスウェイ図:がん微小環境における免疫チェックポイントシグナル伝達
T細胞は免疫応答における主要なエフェクター細胞であるため、その応答を制御するLAG-3 (lymphocyte-activation gene 3)、PD-1 (programmed cell death protein 1)、CTLA-4 (cytotoxic T-lymphocyte-associated protein 4) などの、複数の自己抑制性細胞表面受容体を発現しています。腫瘍細胞は、がん微小環境において、これらの受容体に対するリガンドを上方制御することにより腫瘍の耐性を強化し、免疫系による排除を回避しています。
近年、免疫チェックポイント療法として知られるこれらのリガンド-受容体相互作用の薬理学的なモジュレーターの研究が進められており、がん治療のための新たな免疫療法剤として活用されています。特に興味深いのは、PD-1およびCTLA-4に対するモノクローナル抗体です。これらの免疫チェックポイント療法は、開発初期に抗腫瘍免疫応答を活性化することに成功したため、他の共抑制受容体および共刺激受容体と、そのリガンドを標的とする免疫療法もまた、有望な治療戦略として期待されています。
その他のリソース
- がんの特性研究の標的に関する、完全なガイドをご覧ください。eBookをダウンロードする
詳細は「がんの特性」シリーズのブログをご覧ください。
参考文献
- Hanahan D, Weinberg RA (January 2000). "The Hallmarks of Cancer". Cell. 100 (1): 57–70. doi:10.1016/S0092-8674(00)81683-9
- Hanahan D, Weinberg RA (March 2011). "Hallmarks of Cancer: the next generation". Cell. 144 (5):646-74. doi: 10.1016/j.cell.2011.02.013.
- Sharma P, Allison JP. The future of immune checkpoint therapy. 2015;348(6230):56-61